题目内容
17. 小明测定一瓶稀盐酸的溶质质量分数,具体步骤如下:
小明测定一瓶稀盐酸的溶质质量分数,具体步骤如下:步骤一:配制溶质质量分数为10%的氢氧化钠溶液
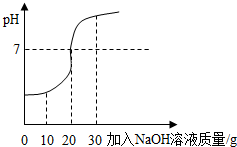
步骤二:向50克待测稀盐酸中逐渐滴入上述氢氧化钠溶液,并使用pH传感器记录溶液的pH变化情况,绘制图象如图.
(1)在往盐酸中逐渐滴入氢氧化钠溶液的过程中,当溶液的pH达到10时,溶液中的溶质的NaCl、NaOH.(用化学式表示)
(2)请结合如图,计算该稀盐酸的溶质质量分数为多少?(写出计算过程)
分析 稀盐酸和氢氧化钠反应生成氯化钠和水,根据提供的数据可以进行相关方面的计算.
解答 解:(1)当溶液的pH达到10时,氢氧化钠过量,溶液中的溶质有反应生成的氯化钠和没有反应的氢氧化钠,氯化钠和氢氧化钠的化学式分别是NaCl、NaOH.
故填:NaCl、NaOH;
(2)设50g稀盐酸中氯化氢的质量为x,
由图中数据可知,加入20g氢氧化钠溶液时恰好完全反应,
NaOH+HCl═NaCl+H2O,
40 36.5
20g×10% x
$\frac{40}{36.5}=\frac{20g×10%}{x}$
x=1.825g
该稀盐酸的溶质质量分数为:$\frac{1.825g}{50g}×100%$=3.65%
答:该稀盐酸的溶质质量分数为3.65%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,同时考查了分析数据的能力,计算时要注意规范性和准确性.

练习册系列答案
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
8. 通过分析组成和结构,可以预测物质的某些性质.根据如图硫酸氢钠溶液的微观示意图,分析推测 NaHSO4的性质,其中不合理的是( )
通过分析组成和结构,可以预测物质的某些性质.根据如图硫酸氢钠溶液的微观示意图,分析推测 NaHSO4的性质,其中不合理的是( )
 通过分析组成和结构,可以预测物质的某些性质.根据如图硫酸氢钠溶液的微观示意图,分析推测 NaHSO4的性质,其中不合理的是( )
通过分析组成和结构,可以预测物质的某些性质.根据如图硫酸氢钠溶液的微观示意图,分析推测 NaHSO4的性质,其中不合理的是( )| A. | 其水溶液能与金属钾发生置换反应,得到金属钠 | |
| B. | 其水溶液能使紫色石蕊试液变红 | |
| C. | 其水溶液能与金属锌反应生成氢气 | |
| D. | 其水溶液与硝酸钡溶液反应生成硫酸钡沉淀 |
9.下列有关实验的评价正确的是( )
| A. | 点燃某可燃物,在火焰上罩一个干冷的烧杯,内壁有水雾出现,则可燃物一定含有H2 | |
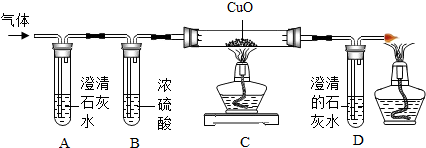
| B. | 某混合气体能使灼热的氧化铜变成红色固体,且导出后气体能使澄清石灰水变浑浊,证明原气体中一定含有一氧化碳 | |
| C. | 在任何实验操作中,绝不可以将滴管伸入盛放被滴加药品的试管中 | |
| D. | 实验室用大理石与盐酸反应制取的CO2通入澄清石灰水无沉淀生成,可能是因为盐酸太浓 |
 工业生产产生的烟气中通常含有二氧化硫,若直接排放会造成空气污染.因此在排放前需要经脱硫处理.如图是两处常用脱硫工艺中含硫物质的转化路径(部分产物已省略).
工业生产产生的烟气中通常含有二氧化硫,若直接排放会造成空气污染.因此在排放前需要经脱硫处理.如图是两处常用脱硫工艺中含硫物质的转化路径(部分产物已省略).