题目内容
2.人被蚊虫叮咬后,蚊虫分泌出蚁酸,使叮咬处又痛又痒.化学小组同学对蚁酸产生了浓厚的兴趣,决定对其进行探究.【提出问题】蚁酸的成分是什么?它有什么性质?
【查阅资料】Ⅰ.蚁酸是一种有机酸,化学名称叫做甲酸,化学式为HCOOH;
Ⅱ.蚁酸在隔绝空气并加热的条件下会分解生成两种氧化物.
【实验探究】
[探究一]向盛有蚁酸溶液的试管中滴加试液,观察到溶液颜色变成红色,说明蚁酸溶液显酸性;
[探究二]小芳同学根据蚁酸的组成元素,推测出一种生成物是水;生成的另一种氧化物是气体,小敏提出两种猜想:猜想Ⅰ:该气体是CO2;
猜想Ⅱ:该气体是CO.
[探究三]他们将蚁酸分解产生的气体通过如图的装置.
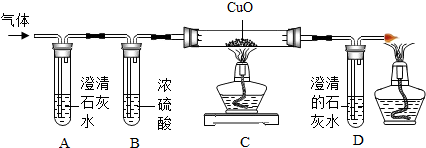
实验时装置A中无明显变化,则猜想Ⅰ不成立(填“成立”或“不成立”);若猜想Ⅱ成立,则:
①实验时装置C中的现象是黑色粉末变成红色;
②实验时装置D中发生反应的化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O;
【实验结论】甲酸受热分解的化学方程式是HCOOH$\frac{\underline{\;\;△\;\;}}{\;}$CO+H2O.
【思维拓展】①当你被蚊虫叮咬后,在叮咬处涂抹一些物质可减轻痛痒.下列物质中,你不会选择的物质是B.
A.氨水 B.肥皂水 C.苏打水 D.烧碱溶液
②向某溶液中加入蚁酸有气泡产生,该气体能使澄清石灰水变浑浊,则该溶液中溶质的化学式可能是Na2CO3(或其它可溶性碳酸盐、酸式碳酸盐等)(合理即可)(只写一种).
分析 【探究二】根据蚁酸的化学式为HCOOH,可知分解的气体可能是一氧化碳或二氧化碳;
【探究三】装置A中无明显变化判断是否成立;
①根据气体肯定是CO,根据CO可以还原CuO判断C中的现象;根据二氧化碳能使澄清石灰水变浑浊解答;
【实验结论】
根据反应原理写出反应的化学方程式解答;
【思维拓展】
(1)从甲酸显酸性考虑;
(2)把“该气体能使澄清石灰水变浑浊,”作为突破口.
解答 解:
[探究二]蚁酸在一定条件下会分解生成两种氧化物,该气体可能是CO2,该气体可能是CO;
[探究三]实验时装置A中无明显变化,说明没有二氧化碳,则猜想I不成立;
①装置C中的现象是黑色粉末变成红色;
②装置D中石灰水变浑浊,说明是一氧化碳,发生反应的化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O;
【实验结论】甲酸受热分解的化学方程式是:HCOOH$\frac{\underline{\;\;△\;\;}}{\;}$CO+H2O;
【思维拓展】
(1)因为甲酸显酸性,不能用食醋处理.故填:B.
(2)向某溶液中加入蚁酸有气泡产生,该气体能使澄清石灰水变浑浊,则该溶液中溶质是碳酸盐.故填:Na2CO3(或其它可溶性碳酸盐、酸式碳酸盐等).
答案:
[探究二]CO;
[探究三]不成立;
①黑色粉末变成红色;
②Ca(OH)2+CO2=CaCO3↓+H2O;
【实验结论】HCOOH$\frac{\underline{\;\;△\;\;}}{\;}$CO+H2O;
【思维拓展】
①B;
②Na2CO3(或其它可溶性碳酸盐、酸式碳酸盐等).
点评 解答本题的关键是要充分理解实验装置的特点和各种物质的性质,只有这样才能对问题做出正确的判断.

练习册系列答案
相关题目
12.下列图示实验操作中,正确的是( )
| A. |  读液体体积 | B. |  称量固体质量 称量固体质量 | C. |  过滤 | D. |  稀释浓硫酸 |
10.为了测定某碳酸钠样品中杂质氯化钠的质量分数,李明同学进行了三次实验,实验数据如表:
完成下列计算:
(1)碳酸钠样品中氯化钠的质量是多少?
(2)碳酸钠样品中杂质氯化钠的质量分数是多少?
| 编 号 | 第1次 | 第2次 | 第3次 |
| 所取固体样品的质量/g | 7 | 5 | 5 |
| 加入氯化钙溶液的质量/g | 50 | 50 | 75 |
| 反应后生成沉淀的质量/g | 4 | 4 | 4 |
(1)碳酸钠样品中氯化钠的质量是多少?
(2)碳酸钠样品中杂质氯化钠的质量分数是多少?
14.下列实验操作中,正确的是( )
| A. |  滴管用后不洗涤 | B. |  过滤 | C. |  稀释浓硫酸 | D. | 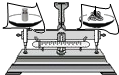 称量固体 |
11.按下列装置实验,操作错误的是( )
| A. | 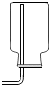 收集H2 | B. | 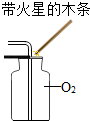 O2验满 | ||
| C. | 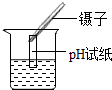 测溶液的PH值 | D. | 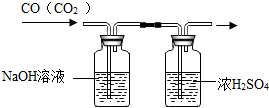 除去CO中的CO2 |
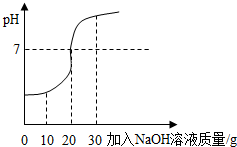 小明测定一瓶稀盐酸的溶质质量分数,具体步骤如下:
小明测定一瓶稀盐酸的溶质质量分数,具体步骤如下: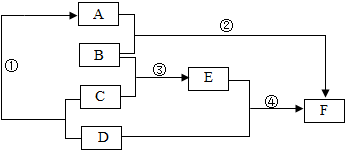 如图是初中化学中六种常见物质之间的转化关系图.
如图是初中化学中六种常见物质之间的转化关系图.