题目内容
16.硬水中含有较多的Mg2+、Ca2+,常用肥皂水区分硬水和软水,生活中既能降低水的硬度,又能杀菌消毒的“84消毒液”的主要成分是次氯酸钠(NaClO),制备其的化学方程式可表示为:2NaOH+X═NaClO+NaCl+H20,则X的化学式为C12,在NaClO中氯元素的化合价为+1.分析 硬水是指含有较多可溶性钙、镁化合物的水;根据化学反应前后原子的种类和数目不变可以判断反应的化学方程式中某物质的化学式;根据化合物中各元素的化合价的代数和为零分析.
解答 解:通常可用肥皂水来检验硬水与软水,其中产生泡沫较多的是软水,泡沫较少的是硬水;
根据反应的化学方程式2NaOH+X═NaClO+NaCl+H2O,反应前含有2个Na原子,2个H原子,2个O原子,以及X,反应后含有2个Na原子,2个H原子,2个O原子,2个Cl原子,故X中含有2个Cl原子,故其化学式为Cl2;NaClO中钠的化合价为+1价、氧为-2价,NaClO中,钠元素的化合价是+1价,氧元素的化合价是-2价,设Cl元素的化合价为x,则(+1)+x+(-2)=0,则x=+1价;
故答案为:肥皂水;C12;+1.
点评 题目难度不大但涉及知识点较多,养成勤于归纳、对比的习惯对于解答类似问题会有较大帮助.

练习册系列答案
相关题目
1.下列关于资源、能源的叙述正确的是( )
| A. | 使化石燃料充分燃烧,既可以减少空气污染.又可以节约化石能源 | |
| B. | 空气的成分按体积计大约是:氮气和氧气占99%,稀有气体占1% | |
| C. | 海洋蕴藏着丰富的化学资源,目前测定海水中含有的物质有80多种 | |
| D. | 人类可直接利用的淡水资源占全球总储水量的2.53% |
8.下列物质间的转化,不能一步实现的是( )
| A. | O2→H2O | B. | H2SO4→HCl | C. | Ca(OH)2→CaCO3 | D. | NaNO3→NaCl |
5.下列现象中一定发生化学变化的是( )
| A. | 木材燃烧 | B. | 湿衣服晾干 | C. | 矿石粉碎 | D. | 用麻织布 |
6.下列性质属于化学性质的是( )
| A. | 金刚石是天然存在的最硬的物质 | |
| B. | 铜具有良好的导电性、导热性、延展性 | |
| C. | 生铁在潮湿的空气中容易生锈 | |
| D. | 二氧化硫具有刺激性气味 |
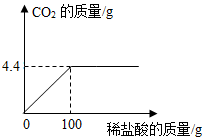 某化学兴趣小组欲测定碳酸钙样品的纯度(杂质不与盐酸反应)取12.5g样品加入到稀盐酸中,产生CO2的质量与稀盐酸的质量关系如图所示,请回答:
某化学兴趣小组欲测定碳酸钙样品的纯度(杂质不与盐酸反应)取12.5g样品加入到稀盐酸中,产生CO2的质量与稀盐酸的质量关系如图所示,请回答: