题目内容
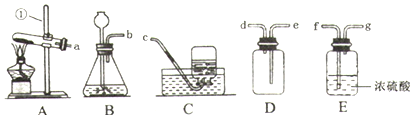
19.现有铜与金属镁、铁、锌中的一种组成的混合物,现欲测定其组成.【实验步骤及数据】取该混合物粉末8.0 g放入烧杯中,将140.0g 溶质质量分数为14.0%的稀硫酸平均分四次加入该烧杯中,充分反应后,测得剩余固体质量数据记录如图2:
(1)该混合物粉末中铜的质量分数是52.5%;
(2)实验室有一瓶浓硫酸,仔细观察标签:
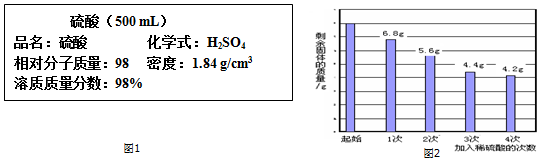
现要将10g这种浓硫酸稀释成实验所用的稀硫酸,问需要加水质量为多少?
分析 根据图中提供的数据可以判断铜的质量,进一步可以计算铜的质量分数;
溶液稀释前后,溶质质量不变.
解答 解:(1)由图中数据可知,铜质量是4.2g,该混合物粉末中铜的质量分数是:$\frac{4.2g}{8.0g}$×100%=52.5%,
故填:52.5%.
(2)要将10g这种浓硫酸稀释成实验所用的稀硫酸,问需要加水质量为:10g×98%÷14.0%-10g=60g,
答:要将10g这种浓硫酸稀释成实验所用的稀硫酸,问需要加水质量为60g.
点评 本题主要考查学生进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.下列物质名称、俗名、化学式、物质类别完全对应的是( )
| A. | 碳酸钙、熟石灰、CaCO3、盐 | B. | 碳酸钠、纯碱、Na2CO3、碱 | ||
| C. | 氢氧化钙、生石灰、Ca(OH)2、碱 | D. | 氢氧化钠、苛性钠、NaOH、碱 |
7.金属R投入硫酸铜溶液中,有红色固体析出;镁条插入R的硫酸盐溶液中,有R析出,则R、Mg、Cu的金属活动性顺序是( )
| A. | Mg>R>Cu | B. | Cu>R>Mg | C. | R>Mg>Cu | D. | Mg>Cu>R |
11.如图是甲、乙两物质的溶解度曲线.下列说法中正确的是( )


| A. | 若将t1℃时的甲、乙的饱和溶液升温至t2℃时,乙溶液中溶质的质量分数将大于甲溶液中溶质的质量分数 | |
| B. | t2℃时,甲、乙的饱和溶液中含有的溶质质量甲等于乙 | |
| C. | 若将t3℃的甲、乙的饱和溶液分别降温到t2℃时,甲、乙两溶液中均有晶体析出 | |
| D. | 当甲中混有少量乙时,可采用冷却热饱和溶液的方法提纯 |
8.用食盐晶体配制溶质质量分数一定的氯化钠溶液,应选用的一组仪器是( )
①量筒 ②酒精灯 ③玻璃棒 ④托盘天平 ⑤蒸发皿 ⑥烧杯.
①量筒 ②酒精灯 ③玻璃棒 ④托盘天平 ⑤蒸发皿 ⑥烧杯.
| A. | ②③⑤⑥ | B. | ①③⑤⑥ | C. | ①③④⑥ | D. | ①④⑤⑥ |
9.工业制取硅的其中一步反应原理是SiCl4+2H2$\frac{\underline{\;高温\;}}{\;}$Si+4HCl,该反应属于基本反应类型中的( )
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |