题目内容
11.如图是甲、乙两物质的溶解度曲线.下列说法中正确的是( )
| A. | 若将t1℃时的甲、乙的饱和溶液升温至t2℃时,乙溶液中溶质的质量分数将大于甲溶液中溶质的质量分数 | |
| B. | t2℃时,甲、乙的饱和溶液中含有的溶质质量甲等于乙 | |
| C. | 若将t3℃的甲、乙的饱和溶液分别降温到t2℃时,甲、乙两溶液中均有晶体析出 | |
| D. | 当甲中混有少量乙时,可采用冷却热饱和溶液的方法提纯 |
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:A、甲、乙物质的溶解度随温度的升高而增大,t1℃时的甲物质的溶解度大于乙物质的溶解度,甲物质饱和溶液的溶质质量分数大于乙物质饱和溶液的质量分数,所以若将t1℃时的甲、乙的饱和溶液升温至t2℃时,乙溶液中溶质的质量分数将小于甲溶液中溶质的质量分数,故A错误;
B、t2℃时,甲、乙物质的溶解度相等,但是甲、乙的饱和溶液的质量不能确定,所以饱和溶液中含有的溶质质量也不能确定,故B错误;
C、甲、乙物质的溶解度随温度的降低而减小,所以若将t3℃的甲、乙的饱和溶液分别降温到t2℃时,甲、乙两溶液中均有晶体析出,故C正确;
D、甲物质的溶解度受温度的变化影响较小,所以当甲中混有少量乙时,可采用蒸发结晶的方法提纯,故D错误.
故选:C.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
1.下列物质充分混合后不能形成溶液的是( )
| A. | 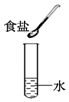 | B. | 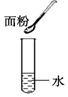 | C. | 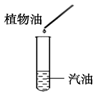 | D. | 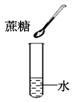 |
2.X,Y,Z三种常见金属存在以下反应,①X+H2SO4=XSO4+H2↑ ②Y+H2SO4不发生反应
③Y+2ZNO3=Y(NO3)2+2Z,则三种金属的活动性顺序正确的是( )
③Y+2ZNO3=Y(NO3)2+2Z,则三种金属的活动性顺序正确的是( )
| A. | Y>X>Z | B. | X>Z>Y | C. | X>Y>Z | D. | Z>X>Y |
6.下列有关玻璃导管的使用图示正确的是(省略夹持和加热装置)( )
| A. | 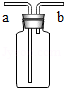 排空气法收集氧气,从a端进 | B. |  排水集气法 | ||
| C. | 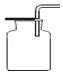 向上排空气法 | D. | 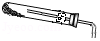 用高锰酸钾制氧气 |
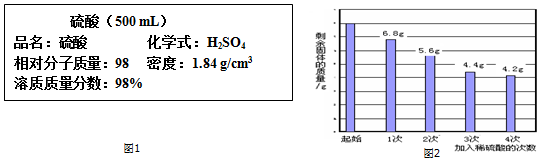
16.石灰石是主要矿产之一,小明同学为了测定石灰石中CaCO3的质量分数,取来了一些石灰石样品,并取稀盐酸进行三次实验,结果如下:
(1)哪几次反应中盐酸有剩余?1、2.
(2)分析上表三次实验可知,10克石灰石样品中的CaCO3恰好完全反应时,消耗稀盐酸的质量是80克.
(3)试计算这种石灰石矿中碳酸钙的质量分数.
| 实验次数 | 1 | 2 | 3 |
| 加入样品的质量╱克 | 10 | 10 | 20 |
| 加入稀盐酸的质量╱克 | 100 | 120 | 80 |
| 生成CO2 的质量╱克 | 3.52 | 3.52 | 3.52 |
(2)分析上表三次实验可知,10克石灰石样品中的CaCO3恰好完全反应时,消耗稀盐酸的质量是80克.
(3)试计算这种石灰石矿中碳酸钙的质量分数.
3.某校同学开展了如下“溶液酸碱性的检验”的实验活动:

(1)把自制的紫色紫薯汁按图1所示分别滴加到试管中,观察到的现象如表所示:
据上表推测,紫薯汁能做酸碱指示剂,遇到稀硫酸溶液可能显示的颜色是红色;
(2)图2是三位同学分别测定土壤酸碱度的操作示意图,其中正确的是B(填“A”“B”或“C”,下同),可能导致溶液pH数值发生改变的错误操作是C.

(1)把自制的紫色紫薯汁按图1所示分别滴加到试管中,观察到的现象如表所示:
| 溶液 | 白醋 | 盐酸 | 蔗糖水 | 草木灰水 | 石灰水 |
| 加入紫薯汁后的颜色 | 红色 | 红色 | 紫色 | 绿色 | 绿色 |
(2)图2是三位同学分别测定土壤酸碱度的操作示意图,其中正确的是B(填“A”“B”或“C”,下同),可能导致溶液pH数值发生改变的错误操作是C.
1.规范的操作是确保实验成功的关键.下列所示的操作中,正确的是( )
| A. | 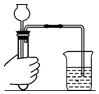 检查气密性 | B. | 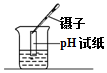 测量溶液的pH | C. | 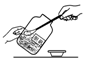 取固体药品 | D. | 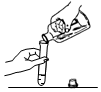 取少量液体 |
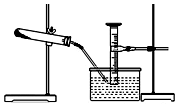 某学生用胆矾制取氧化铜固体,并研究氧化铜能否在氯酸钾受热分解实验中起催化作用.实验步骤如下:①称量a g胆矾固体放入烧杯中,加水配制成溶液,向其中滴加氢氧化钠溶液至沉淀完全,过滤;②把步骤①中的滤渣转移至蒸发皿中,加热至全部变成黑色氧化铜为止;③过滤、洗涤、干燥、称量所得固体质量为b g;④分别取一定质量的上述氧化铜固体和氯酸钾固体混合均匀,如图所示,加热、收集反应生成的氧气.
某学生用胆矾制取氧化铜固体,并研究氧化铜能否在氯酸钾受热分解实验中起催化作用.实验步骤如下:①称量a g胆矾固体放入烧杯中,加水配制成溶液,向其中滴加氢氧化钠溶液至沉淀完全,过滤;②把步骤①中的滤渣转移至蒸发皿中,加热至全部变成黑色氧化铜为止;③过滤、洗涤、干燥、称量所得固体质量为b g;④分别取一定质量的上述氧化铜固体和氯酸钾固体混合均匀,如图所示,加热、收集反应生成的氧气.