题目内容
2.如图是自来水厂净水过程示意图.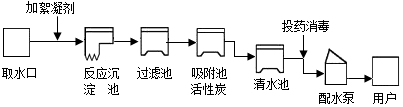
请根据图示回答下列问题
①自来水厂生产自来水时,使用的净水方法有下列方法中的ABE.(填写字母序号)
A.沉淀 B.过滤 C.煮沸 D.蒸馏 E.吸附
②自来水厂常用二氧化氯进行投药消毒,二氧化氯中氯元素的化合价为+4.漂白粉可用于水的杀菌消毒,其有效成分是次氯酸钙[化学式为Ca(ClO2)].次氯酸钙可发生如下反应:Ca(ClO)2+X+H2O═CaCO3↓+2HClO则X的化学式为CO2.
(2)水在直流电的作用下发生分解的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,在实验中若负极产生的气体的体积是20mL,则正极产生的气体的体积约是10mL.
分析 (1)可以根据净化水的方法方面进行分析、考虑,从而得出正确的结论;
(2)根据质量守恒定律反应前后原子的种类及数目不变分析判断X的化学式.根据化合价原则可计算出二氧化氯中氯元素的化合价.
(3)根据写方程式的步骤写,不要忘了注明反应条件,由氢气和氧气的体积比为2:1得出氧气体积;
解答 解:(1)自来水厂生产自来水时,使用的净水方法有沉淀、过滤、吸附.故填:ABE.
(2)设二氧化氯中氯元素的化合价为x.则x+(-2)×2=0,解得x=+4.
根据所给化学方程式可以看出:化学方程式的右边比左边多出了1个碳原子和2个氧原子;
根据质量守恒定律中的元素种类不变和原子个数不变的特点,可知多出的原子全部来自1个X分子中,即X的化学式为CO2.
(3)水在直流电的作用下发生分解的化学方程式中反应物为水,生成物为氢气和氧气,反应条件是通电,化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;由氢气和氧气的体积比为2:1,负极产生的气体是氢气,体积是20mL,则正极产生的气体氧气的体积是10mL;
答案:
(1)①ABE; ②+4; CO2; (2)2H2O$\frac{\underline{\;通电\;}}{\;}$ 2H2↑+O2↑;10;
点评 本题考查了净水的知识,完成此题,可以依据已有的知识进行解答,属于基础知识,难度中等.能够把图中信息和化学知识有机的结合起来.

练习册系列答案
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
12.俗话说”人要实心,火要空心”.下列对“火要空心”的目的理解正确的是( )
| A. | 增大可燃物与氧气的接触面积 | B. | 隔绝空气 | ||
| C. | 降低可燃物的着火点 | D. | 移除木柴使火熄灭 |
13.分离、除杂、提纯和检验是化学实验的重要环节,下面实验设计能达到实验目的是( )
| 实验内容 | 实验设计 | |
| A | 除去CO2中少量水蒸气、HCl气体 | 先通过浓硫酸、再通过NaOH溶液 |
| B | 除去NaCl中难溶性杂质 | 溶解、过滤、蒸发 |
| C | 除去KCl溶液中少量的K2CO3 | 加入适量Ca(NO3)2溶液、过滤 |
| D | 除去硫酸钾溶液中的硫酸镁 | 滴加适量的氢氧化钠溶液 |
| A. | A | B. | B | C. | C | D. | D |
14.最近新闻报道,由于气候变暖,南极冰川以前所未有的速度融化.下列气体中能引起气候变暖的是( )
| A. | O2 | B. | N2 | C. | CO2 | D. | SO2 |
11. 如图所示是某反应前后的微观示意图,“
如图所示是某反应前后的微观示意图,“ ”和“
”和“ ”表示两种不同的原子,则下列说法正确的是( )
”表示两种不同的原子,则下列说法正确的是( )
 如图所示是某反应前后的微观示意图,“
如图所示是某反应前后的微观示意图,“ ”和“
”和“ ”表示两种不同的原子,则下列说法正确的是( )
”表示两种不同的原子,则下列说法正确的是( )| A. | 有单质生成 | B. | 是化合反应 | ||
| C. | 反应前后分子种类不变 | D. | 参加反应的两种分子个数比为4:1 |
 如图是A、B、C三种物质的溶解度曲线,请回答
如图是A、B、C三种物质的溶解度曲线,请回答