题目内容
7. 如图是A、B、C三种物质的溶解度曲线,请回答
如图是A、B、C三种物质的溶解度曲线,请回答(1)t1℃时,A、B、C三种物质的溶解度由大到小的顺序是C>B>A;
(2)当A中混有少量B时,可用降温结晶方法提纯A;
(3)t2℃时,在100g水中放入60gA物质恰好形成饱和溶液,此时溶液中溶质的质量分数为37.5%;
(4)要使C的饱和溶液变为不饱和溶液,除加水之外还可采用的方法是降低温度.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)通过分析溶解度曲线可知,t1℃时,A、B、C三种物质的溶解度由大到小的顺序是:C>B>A;
(2)A物质的溶解度受温度影响变化较大,所以当A中混有少量B时,可用降温结晶方法提纯A;
(3)t2℃时,A物质的溶解度是60g,所以在100g水中放入60gA物质恰好形成饱和溶液,此时溶液中溶质的质量分数为:$\frac{60g}{160g}$×100%=37.5%;
(4)C物质的溶解度随温度的降低而增大,所以要使C的饱和溶液变为不饱和溶液,除加水之外还可采用的方法是降低温度.
故答案为:(1)C>B>A;
(2)降温结晶;
(3)60g,37.5%;
(4)降低温度.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
17.下列各组物质除杂方法正确的是( )
| 选项 | 物质(括号内为杂质) | 操作方法 |
| A | NaCl 溶液(Na2SO4) | 加入适量的BaCl2溶液,过滤 |
| B | CaO 固体(CaCO3) | 加入过量的水,过滤 |
| C | O2 (H2) | 把气体通过灼热的铜网 |
| D | CaCl2溶液(稀HCl) | 加入适量的Na2CO3溶液 |
| A. | A | B. | B | C. | C | D. | D |
15.分析推理是化学学习过程中的常用方法,下列推理正确的是( )
| A. | 物质和氧气发生的反应是氧化反应,所以发生氧化反应一定有氧气参加 | |
| B. | 稀有气体元素的原子最外层电子数为8(氦除外),因此微粒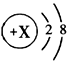 一定是稀有气体元素的原子 一定是稀有气体元素的原子 | |
| C. | 碱性溶液能使酚酞试液变红色,因此能使酚酞试液变红色的溶液的pH一定大于7 | |
| D. | 溶液中有晶体析出时,溶质质量减小,所以溶质的质量分数一定减小 |
12.碳原子的核电荷数为( )
| A. | 8 | B. | 7 | C. | 12 | D. | 6 |
19.下列化肥属于含磷复合肥料的是( )
| A. | NH4NO3 | B. | KNO3 | C. | (NH4)2HPO4 | D. | Ca (H2PO4)2 |
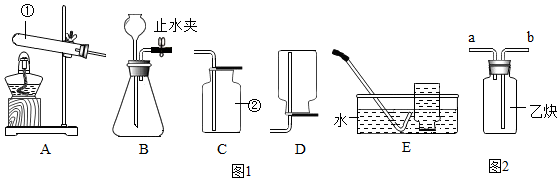
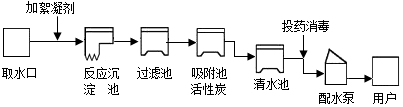
 2016年3月22~28日是第29届“中国水周”,其主体为“落实五大发展理念,推进最严格水资源管理”.
2016年3月22~28日是第29届“中国水周”,其主体为“落实五大发展理念,推进最严格水资源管理”.