题目内容
10.有一包白色固体A,可能含氯化铁、碳酸钙、硫酸钠、氯化钡、氢氧化钡、氢氧化钠中的几种.取少量A做如下实验,主要现象如图所示,请用化学式填空.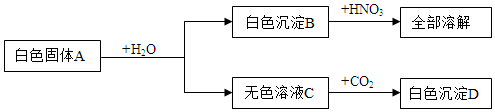
(1)白色沉淀B是CaCO3,D是BaCO3.
(2)白色固体A中一定不存在的物质是FeCl3和Na2SO4.
(3)若白色固体A中只含有两种物质,它们是CaCO3和Ba(OH)2.
(4)白色固体A还有其它哪些可能的组成CaCO3、Ba(OH)2、BaCl2,CaCO3、Ba(OH)2、NaOH,CaCO3、Ba(OH)2、BaCl2、NaOH,CaCO3、BaCl2、NaOH(至少写出两种).
分析 根据氯化铁在溶液中显黄色,硫酸根离子和钡离子反应生成不溶于酸的硫酸钡沉淀,氢氧化钡和二氧化碳反应生成碳酸钡沉淀和水,氢氧化钠和二氧化碳反应生成碳酸钠,碳酸根离子和钡离子反应生成溶于酸的碳酸钡沉淀等知识进行分析.
解答 解:氯化铁在溶液中显黄色,硫酸根离子和钡离子反应生成不溶于酸的硫酸钡沉淀,氢氧化钡和二氧化碳反应生成碳酸钡沉淀和水,氢氧化钠和二氧化碳反应生成碳酸钠,碳酸根离子和钡离子反应生成溶于酸的碳酸钡沉淀.
白色固体A加水溶解后得到白色沉淀B和无色溶液C,所以A中一定不含氯化铁,白色沉淀B中加硝酸,固体全部溶解,所以固体A中一定不含硫酸钠,一定含有碳酸钙,所以
(1)白色沉淀B是CaCO3,D是BaCO3;
(2)白色固体A中一定不存在的物质是:FeCl3和Na2SO4;
(3)固体A中一定含有CaCO3、Ba(OH)2,所以,若白色固体A中只含二种物质,它们是CaCO3、Ba(OH)2;
(4)白色固体A一定含有碳酸钙,还有其它哪些可能的组成是:CaCO3、Ba(OH)2、BaCl2,CaCO3、Ba(OH)2、NaOH,CaCO3、Ba(OH)2、BaCl2、NaOH,CaCO3、BaCl2、NaOH.
故答案为:(1)CaCO3,BaCO3;
(2)FeCl3和Na2SO4;
(3)CaCO3、Ba(OH)2;
(4)CaCO3、Ba(OH)2、BaCl2,CaCO3、Ba(OH)2、NaOH,CaCO3、Ba(OH)2、BaCl2、NaOH,CaCO3、BaCl2、NaOH.
点评 在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可.

练习册系列答案
 全程金卷系列答案
全程金卷系列答案
相关题目
5.请用H、C、O、Cl、Fe、Na六种元素中的一种或几种,按要求完成下列各小题
(1)请写出符合下列要求粒子的化学符号
(2)请写出符合下列要求物质的化学式
(3)用上述六种元素中的一种或几种组成的物质,写出符合下列要求的一个化学反应方程式
(1)请写出符合下列要求粒子的化学符号
| ①两个氧原子 | ②两个氧气分子 | ③两个亚铁离子 |
| 2O | 2O2 | 2Fe2+ |
| ①密度最小的物质 | ②小苏打 | ③可用作燃料的氧化物 |
| H2 | NaHCO3 | CO |
| ①难溶性的碱受热分解生成对应的金属氧化物和水 | ②中和反应 |
| 2Fe(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Fe2O3+3H2O | NaOH+HCl=NaCl+H2O |
15.分析推理是化学学习过程中的常用方法,下列推理正确的是( )
| A. | 物质和氧气发生的反应是氧化反应,所以发生氧化反应一定有氧气参加 | |
| B. | 稀有气体元素的原子最外层电子数为8(氦除外),因此微粒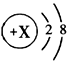 一定是稀有气体元素的原子 一定是稀有气体元素的原子 | |
| C. | 碱性溶液能使酚酞试液变红色,因此能使酚酞试液变红色的溶液的pH一定大于7 | |
| D. | 溶液中有晶体析出时,溶质质量减小,所以溶质的质量分数一定减小 |
19.下列化肥属于含磷复合肥料的是( )
| A. | NH4NO3 | B. | KNO3 | C. | (NH4)2HPO4 | D. | Ca (H2PO4)2 |
20.根据下表回答问题.
(1)20℃时,溶解度最大的物质是NH4Cl;
(2)50℃时,在100g水中放入36g氯化钠充分溶解,待温度降到40℃,得到的是氯化钠的不饱和溶液(选填“饱和”或“不饱和”).
| 温度(℃) | 20 | 40 | 50 | 60 | 80 | |
| 溶解度(g) | NaCl | 36.0 | 36.6 | 37.0 | 37.3 | 38.4 |
| NH4Cl | 37.2 | 45.8 | 50.4 | 55.2 | 65.6 | |
| KNO3 | 31.6 | 63.9 | 85.5 | 110 | 169 | |
(2)50℃时,在100g水中放入36g氯化钠充分溶解,待温度降到40℃,得到的是氯化钠的不饱和溶液(选填“饱和”或“不饱和”).