题目内容
14.要除去FeSO4中含有的CuSO4杂质.可以在其溶液中加入铁粉,反应的化学方程式是:Fe+CuSO4═FeSO4+Cu.充分反应后,再用过滤方法除去杂质.分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:除去FeSO4中含有的CuSO4杂质,实质就是除去铜离子,可利用CuSO4溶液与足量的铁粉反应生成硫酸亚铁溶液和铜,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu.
故答案为:铁粉;Fe+CuSO4═FeSO4+Cu;过滤.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
5.下列操作或现象与分子对应的特性不一致的是( )
| A. | 给篮球充气,分子之间有间隔 | |
| B. | 夏天湿衣服干的快,温度升高,分子运动加快 | |
| C. | 100ml酒精和100ml水混合后体积小于200ml,分子是有质量的 | |
| D. | 在花园中可闻到花的香味,分子是运动的 |
4.向硝酸银、硝酸铜、硝酸镁的混合溶液中加入一些铁粉,待充分反应后,再过滤.下列情况不可能存在的是( )
| A. | 滤纸上有银,滤液中有Cu2+、Ag+、Fe2+、Mg2+ | |
| B. | 滤纸上有Cu、Ag,滤液中有Fe2+、Mg2+ | |
| C. | 滤纸上有Cu、Ag,滤液中有Ag+、Fe2+、Mg2+ | |
| D. | 滤纸上有Fe、Cu、Ag,滤液中有Fe2+、Mg2+ |
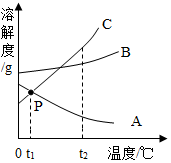 如图是A、B、C三种物质的溶解度曲线,据图回答:
如图是A、B、C三种物质的溶解度曲线,据图回答:
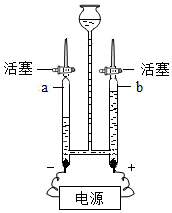 水是人类生活中不可缺少的物质.
水是人类生活中不可缺少的物质.