题目内容
16.标出下列物质中除氢、氧化外其他元素的化合价.| CO2 | Cu | SO3 | H2S | P2O5 | Fe2O3 | N2O3 | SiO2 | Cu(OH)2 |
| K2O | MgO | HNO3 | AgCl | Na2CO3 | BaCl2 | CaO | AlCl3 | ZnSO4 |
分析 根据单质中元素的化合价为零、在化合物中正负化合价代数和为零,进行解答.
解答 解:设中二氧化碳中氮元素的化合价为x,氧显-2价,根据在化合物中正负化合价代数和为零可得:x+(-2)×2=0,则x=+4;根据单质中元素的化合价为0,所以铜中铜元素的化合价为0;
设三氧化硫中硫元素的化合价为y,氧显-2价,根据在化合物中正负化合价代数和为零可得:y+(-2)×3=0,则y=+6;设硫化氢中硫元素的化合价为z,氢显+1价,根据在化合物中正负化合价代数和为零可得:(+1)×2+z=0,则z=-2;
设五氧化二磷中磷元素的化合价为m,氧显-2价,根据在化合物中正负化合价代数和为零可得:2m+(-2)×5=0,则m=+5.同理可计算出氧化铁中铁元素的化合价是+3;三氧化二氮中氮元素的化合价是+3;二氧化硅中硅元素的化合价是+4;氢氧化铜中铜元素的化合价是+2;氧化钾中钾元素的化合价是+1;氧化镁中镁元素的化合价是+2;硝酸中氮元素的化合价是+5;氯化银中银元素和氯元素的化合价分别是+1、-1;碳酸钠中碳元素的化合价是+4;氯化钡中钡元素和氯元素的化合价分别是+2、-1;氧化钙中钙元素的化合价是+2;氯化铝中铝元素和氯元素的化合价分别是+3、-1;硫酸锌中锌元素和硫元素的化合价分别是+2、+6;故填:+4;0;+6;-2;+5;+3;+3;+4;+2;+1;+2;+2、-1;+2;+3、-1;+2、+6.
点评 本题考查根据在化合物中正负化合价代数和为零计算指定元素化合价的解题能力.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
10.t℃时,NaCl溶解于水的实验数据如表所示:
(1)实验③④所得的溶液是饱和溶液;
(2)实验③所得溶液的溶质质量分数为26.5%;
(3)t℃时,NaCl的溶解度为36g.
| 实验序号 | 水的质量/g | 加入NaCl的质量/g | 溶液的质量/g |
| ① | 10 | 2 | 12 |
| ② | 10 | 3 | 13 |
| ③ | 10 | 4 | 13.6 |
| ④ | 10 | 5 | 13.6 |
(2)实验③所得溶液的溶质质量分数为26.5%;
(3)t℃时,NaCl的溶解度为36g.
11.下列化合物中,硫元素显+6价的是( )
| A. | H2S | B. | H2SO3 | C. | H2SO4 | D. | SO2 |
1.在FeO、Fe2O3和CaCO3三种物质组成的混合物中,已知铁元素的质量分数为56%,则在该混合物中钙元素的质量分数可能是( )
| A. | 35% | B. | 25% | C. | 20% | D. | 10% |
8.20℃时,NaCl溶解于水的实验数据如下表.则下列叙述正确的是( )
| 实验序号 | ① | ② | ③ | ④ |
| 水的质量(g) | 10 | 10 | 10 | 10 |
| 加入NaCl的质量(g) | 2 | 3 | 4 | 5 |
| 溶液的质量(g) | 12 | 13 | 13.6 | 13.6 |
| A. | ②中所得溶液是饱和溶液 | B. | 20℃时10g水最多能溶解4gNaCl | ||
| C. | ③④溶液的浓度相同 | D. | ④溶液是不饱和溶液 |
5.我市天山汉墓出土青铜器表面一些有绿色物质,该物质俗称“铜锈”,其化学组成为aCuCO3•bCu(OH)2•cH2O(a、b、c为最简整数比).小红同学为测定其组成,称取该绿色物质25.8g进行如下实验:

已知:Ⅰ、CuCO3$\frac{\underline{\;\;△\;\;}}{\;}$CuO+CO2↑;Ⅱ、Cu(OH)2 $\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O
Ⅲ、图中B处为两个单向阀:推注射器时A1关闭,A2处打开;拉注射器时,A1打开进空气,A2关闭.
(一)实验步骤 ①组装好装置,检查气密性②反复推拉注射器③称量E、F的质量④关闭弹簧夹,加热D处试管直到反应不再进行⑤打开弹簧夹,再次反复缓缓推拉注射器⑥再次称量E、F的质量.
(二)问题探究:
(1)E中的药品为浓硫酸,E的作用是吸收水蒸气.C、F、G中装有碱石灰(CaO与NaOH的固体混合物),则C的作用是除去空气中的二氧化碳,F的作用是吸收生成的二氧化碳,G的作用是防止空气的二氧化碳和水蒸气进入F装置.
(2)实验步骤②与③能否颠倒不能(填“能”或“不能”).若不进行步骤⑤的操作,则所测得的碳酸铜质量分数偏小(填“偏大”、“偏小”、“无影响”),该操作中推注射器时缓缓的目的是使生成的二氧化碳、水蒸气吸收充分.

已知:Ⅰ、CuCO3$\frac{\underline{\;\;△\;\;}}{\;}$CuO+CO2↑;Ⅱ、Cu(OH)2 $\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O
Ⅲ、图中B处为两个单向阀:推注射器时A1关闭,A2处打开;拉注射器时,A1打开进空气,A2关闭.
(一)实验步骤 ①组装好装置,检查气密性②反复推拉注射器③称量E、F的质量④关闭弹簧夹,加热D处试管直到反应不再进行⑤打开弹簧夹,再次反复缓缓推拉注射器⑥再次称量E、F的质量.
(二)问题探究:
| 反应前 | 反应后 |
| E的质量为100.0g | E的质量为105.4g |
| F的质量为50.0g | F的质量为54.4g |
(2)实验步骤②与③能否颠倒不能(填“能”或“不能”).若不进行步骤⑤的操作,则所测得的碳酸铜质量分数偏小(填“偏大”、“偏小”、“无影响”),该操作中推注射器时缓缓的目的是使生成的二氧化碳、水蒸气吸收充分.
6.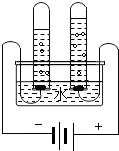 如图为验证水的组成的实验装置,下列有关说法正确的是( )
如图为验证水的组成的实验装置,下列有关说法正确的是( )
 如图为验证水的组成的实验装置,下列有关说法正确的是( )
如图为验证水的组成的实验装置,下列有关说法正确的是( )| A. | 正极和负极产生的气体质量比为1:2 | |
| B. | 正极产生的气体能使带火星的木条复燃 | |
| C. | 水是由一个氧元素和两个氢元素组成的 | |
| D. | 该变化中的最小粒子为氢分子和氧分子 |