题目内容
10.t℃时,NaCl溶解于水的实验数据如表所示:| 实验序号 | 水的质量/g | 加入NaCl的质量/g | 溶液的质量/g |
| ① | 10 | 2 | 12 |
| ② | 10 | 3 | 13 |
| ③ | 10 | 4 | 13.6 |
| ④ | 10 | 5 | 13.6 |
(2)实验③所得溶液的溶质质量分数为26.5%;
(3)t℃时,NaCl的溶解度为36g.
分析 由t℃时,NaCl溶解于水的实验数据表可知,10g水中最多能溶解3.6g氯化钠,据此结合饱和溶液、溶质质量分数=$\frac{溶质质量}{溶液质量}×$100%、溶解度的概念(四要素:温度、100g溶剂、饱和状态、单位是克),进行分析解答.
解答 解:(1)由表中数据可知,随着氯化钠的不断加入,溶液的质量在增加,当10g水中溶解了3.6g氯化钠后不再溶解,说明已经达到饱和状态,实验③④所得的溶液是饱和溶液.
(2)实验③所得溶液的溶质质量分数为$\frac{3.6g}{3.6g+10g}×$100%≈26.5%.
(3)溶解度是在一定温度下,某固体溶质在100g溶剂里达到饱和状态所溶解的溶质质量;t℃时,10g水中最多能溶解3.6g氯化钠,则t℃时,NaCl的溶解度为3.6g×$\frac{100g}{10g}$=36g.
故答案为:(1)③④;(2)26.5%;(3)36g.
点评 本题难度不大,掌握饱和溶液的特征、溶质质量分数=$\frac{溶质质量}{溶液质量}×$100%、溶解度的概念是正确解答本题的关键.

练习册系列答案
相关题目
1.下列四个图象分别对应四种操作过程,其中不正确的是( )
| A. | 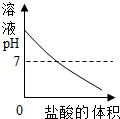 向NaOH溶液中滴加HCl至过量 | |
| B. | 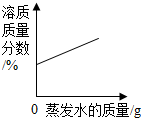 在恒温的条件下,将足量的氯化钠饱和溶液蒸发适量的水分 | |
| C. | 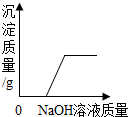 向CuCl2和HCl的混合溶液中加入过量NaOH溶液 | |
| D. | 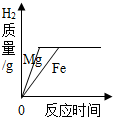 向两份同体积和同质量分数的HCl溶液中分别加入足量的铁粉和镁粉 |
16.标出下列物质中除氢、氧化外其他元素的化合价.
| CO2 | Cu | SO3 | H2S | P2O5 | Fe2O3 | N2O3 | SiO2 | Cu(OH)2 |
| K2O | MgO | HNO3 | AgCl | Na2CO3 | BaCl2 | CaO | AlCl3 | ZnSO4 |
17.下列实验操作不正确的是( )
| A. | 有酒精灯加热试管里的固体时先预热 | |
| B. | 气体发生装置在盛装药品前需检查装置的气密性 | |
| C. | 检查气密性时,先用双手捂住容器外壁后将导管插入水中 | |
| D. | 称量氢氧化钠固体使用小烧杯盛装 |
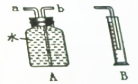 如图A是某学生设计的一种有洗气、贮气等用途的装置.当用排水集气法收集氧气时,瓶内先装满水,将氧气从a(填“a”或“b”,下同)处导管通入.此时用B装置测量b导管口排出的水的体积,就能测出气体的体积.
如图A是某学生设计的一种有洗气、贮气等用途的装置.当用排水集气法收集氧气时,瓶内先装满水,将氧气从a(填“a”或“b”,下同)处导管通入.此时用B装置测量b导管口排出的水的体积,就能测出气体的体积. 如图是初中化学常用的实验仪器,请完成下列各题
如图是初中化学常用的实验仪器,请完成下列各题