题目内容
11.要除去下列物质中的杂质(括号内物质为杂质),下列实验方案设计中合理的是( )| A. | NaCl溶液(Na2SO4):加入过量的BaCl2溶液,过滤 | |
| B. | H2(HCl):将气体通过足量氢氧化钠溶液,再经浓硫酸干燥 | |
| C. | CaO(CaCO3):加水溶解,过滤后洗涤干燥 | |
| D. | NaOH溶液(Na2CO3):加入适量的CaCl2,过滤 |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、Na2SO4能与过量的BaCl2溶液反应生成硫酸钡沉淀和氯化钠,能除去杂质但引入了新的杂质氯化钡(过量的),不符合除杂原则,故选项所采取的方法错误.
B、HCl能与氢氧化钠溶液反应生成氯化钠和水,氢气不与氢氧化钠溶液反应,再经浓硫酸干燥,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
C、CaO能与水反应生成氢氧化钙,碳酸钙难溶于水,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
D、Na2CO3能与适量的CaCl2反应生成碳酸钙沉淀和氯化钠,能除去杂质但引入了新的杂质氯化钠(过量的),不符合除杂原则,故选项所采取的方法错误.
故选:B.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
1.(1)根据表1中相关信息,回答下列问题:
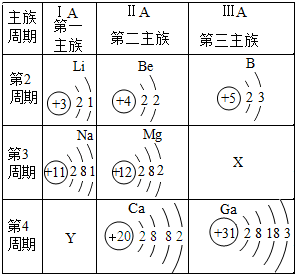
①X处对应原子的最外层电子数为3,Y处对应原子的核外电子层数为4;
②镓原子(Ca)的核外电子数为31,其在化学反应中易失(填“得”或“失”)电子形成镓离子,该离子符号为Ga3+.
(2)物质甲和乙完全反应生成物质丙和丁,各物质的微观示意图如表2所示,下列说法正确的有A
A.甲物质属于有机物
B.该反应属于置换反应
C.反应前后元素的种类增加
D.该反应的化学方程式为:C2H2+3O2═2CO2+2H2O.

①X处对应原子的最外层电子数为3,Y处对应原子的核外电子层数为4;
②镓原子(Ca)的核外电子数为31,其在化学反应中易失(填“得”或“失”)电子形成镓离子,该离子符号为Ga3+.
(2)物质甲和乙完全反应生成物质丙和丁,各物质的微观示意图如表2所示,下列说法正确的有A
| 物质 | 甲 | 乙 | 丙 | 丁 |  |
| 分子示意图 | 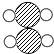 |  |  |
B.该反应属于置换反应
C.反应前后元素的种类增加
D.该反应的化学方程式为:C2H2+3O2═2CO2+2H2O.
2.有一包白色粉末,可能含有氯化钡、氢氧化钠、氯化钠、碳酸钠、硫酸钠、硫酸铜中的一种或几种.为确定其组成,进行下列实验:
①将该白色粉末溶于足量的水中,产生白色沉淀和无色溶液,过滤;
②将滤液分成二等份,向一份中滴加酚酞试液,溶液变红;向另一份中滴加硝酸银溶液,溶液变浑浊;
③将滤渣投入足量的稀盐酸中,白色固体部分溶解并产生大量无色无味的气体.
则下列说法不正确的是( )
①将该白色粉末溶于足量的水中,产生白色沉淀和无色溶液,过滤;
②将滤液分成二等份,向一份中滴加酚酞试液,溶液变红;向另一份中滴加硝酸银溶液,溶液变浑浊;
③将滤渣投入足量的稀盐酸中,白色固体部分溶解并产生大量无色无味的气体.
则下列说法不正确的是( )
| A. | 白色粉末中肯定没有硫酸铜,可能有氢氧化钠和氯化钠 | |
| B. | 白色粉末中肯定有氯化钡、氢氧化钠、硫酸钠和碳酸钠 | |
| C. | 白色粉末中肯定有氯化钡、硫酸钠和碳酸钠,可能有氢氧化钠和氯化钠 | |
| D. | 若在滤液中滴加稀盐酸产生气泡,则白色粉末中肯定有碳酸钠和氯化钡,且二者的质量比可能为$\frac{{m(N{a_2}C{O_3})}}{{m(BaC{l_2})}}$>$\frac{106}{208}$ |
6.下列化学实验操作中,正确的是( )
| A. | 稀释稀硫酸时,把浓硫酸慢慢注入成有水的量筒中,并不断搅拌 | |
| B. | 用漏斗过滤时,使用玻璃棒搅拌,加快过滤速度 | |
| C. | 向燃着的酒精灯里添加酒精 | |
| D. | 点燃氢气等可燃性气体前,一定要检验气体的纯度 |

 “创新”是一个民族的灵魂,是人类发展的不竭动力.
“创新”是一个民族的灵魂,是人类发展的不竭动力.