题目内容
15.按要求填空(1)现有盐酸、水、氮气、浓盐酸、氢氧化钙、硝酸铵、甲烷、生石灰等八种物质,用相应物质的化学式填空:
①非金属气体单质N2; ②具有挥发性的酸HCl;
③可改良酸性土壤的碱Ca(OH)2; ④可作化肥的盐NH4NO3.
(2)水是人们生活生产中应用最多的物质,净化水方法中,净化程度最高的是蒸馏;
硬水中含有较多的③(选填序号);①CaCO3 ②Mg(OH)2 ③Ca2+、Mg2+ ④Na2SO4
(3)用化学用语填空:
构成氯化铝的阴离子Cl-;氧化镁中镁的化合价$\stackrel{+2}{Mg}$O.
(4)用化学方程式表示:
①胃舒平(氢氧化铝)中和过多胃酸Al(OH)3+3HCl═AlCl3+3H2O;
②铜绿受热分解Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$H2O+CO2↑+2CuO.
分析 (1)首先根据题意确定物质的化学名称,然后根据书写化学式的方法和步骤写出物质的化学式即可;
(2)根据净化水的原理以及硬水的概念来分析;
(3)离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.
化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后;
(4)书写化学方程式时,必须熟悉反应物、生成物和反应条件,必须依据客观事实、遵守质量守恒定律.
解答 解:(1)①氮气是一种气态的非金属单质,故填:N2;
②浓盐酸具有强烈的挥发性,故填:HCl;
③氢氧化钙是一种碱,可用于改良酸性土壤;故填:Ca(OH)2;
④硝酸铵这种盐中含有氮元素,是农业上常用的一种氮肥;故填:NH4NO3;
(2)蒸馏可以除去水中的所有杂质,是净化程度最高的方法;硬水中含有较多的可溶性的Ca2+和Mg2+;故填:蒸馏;③;
(3)氯化铝是由铝离子与氯离子构成的化合物,其中阴离子是氯离子,由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.故氯离子表示为Cl-;故填:Cl-;
化合价要标在元素符号的正上方,正负号在前,数值在后;氧化镁中镁元素的化合价表示为$\stackrel{+2}{Mg}$O;故填:$\stackrel{+2}{Mg}$O;
(4)①氢氧化铝和胃酸中的盐酸反应生成氯化铝和水,反应的化学方程式为:Al(OH)3+3HCl═AlCl3+3H2O.故填:Al(OH)3+3HCl═AlCl3+3H2O;
②铜绿为碱式碳酸铜,受热分解产生氧化铜、二氧化碳和水,故填:Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$H2O+CO2↑+2CuO.
点评 本题难度不大,掌握常见化学用语(原子符号、分子符号、化合价、离子符号、化学方程式等)的书写方法、离子符号与化合价表示方法的区别等是正确解答此类题的关键.

| 物质 | 苯 | 氧气 | 二氧化碳 | 水 | X |
| 反应前质量/g | 3.9 | 9.6 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 6.6 | 2.7 | m |
| A. | 表中m的值为4.2 | |
| B. | 物质X由碳、氧元素组成 | |
| C. | 物质X由碳、氢元素,氧元素组成 | |
| D. | 生成二氧化碳和水的分子个数比为2:1 |
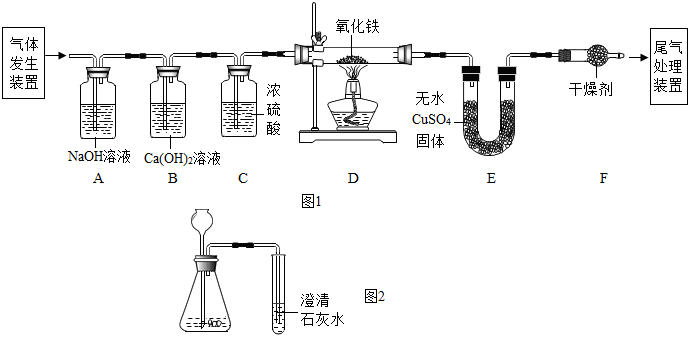
(1)草酸晶体在浓硫酸作用下受热分解,化学方程式为H2C2O4•3H2O$\frac{\underline{\;H_{2}SO_{4}(浓)\;}}{△}$CO2↑+CO↑+4H2O.为证明草酸分解的产物之一是一氧化碳,某兴趣小组的同学用如图1所示装置进行实验研究.
①写出A装置中发生反应的化学方程式为2NaOH+CO2═Na2CO3+H2O.
②B装置的作用是什么?
③证明草酸晶体分解产物中存在CO的现象是什么?
④对D装置加热前要先通入过量的CO,其目的是什么?
(2)在实验室用盐酸和石灰石反应,用如图2所示装置(气密性良好)进行二氧化碳的制取及性质实验,但未发现澄清石灰水变浑浊,针对此现象,同学进行了探究.
【做出猜想】
猜想一:澄清石灰水变质.
猜想二:实验中使用的液体药品是浓盐酸,造成通入石灰水中的气体除了二氧化碳外,还有氯化氢气体.
【实验探究】
| 实验 | 实验步骤 | 实验现象 | 实验结论 |
| 实验Ⅰ | 将纯净的CO2通入该实验所用的澄清石灰水中 | 澄清石灰水变浑浊 | 猜想一不成立 |
| 实验Ⅱ | 将反应产生的气体通入到硝酸银溶液中 | 有白色沉淀产生 | 猜想二成立 |
(1)甲同学将课本的基础知识进行整理如图,请你帮助他完成相关内容.
| 制取气体 | 所需要品 | 装置连接顺序 | 反应化学方程式 |
| 干燥的二氧化碳 | 大理石和稀盐酸 | AED | CaCO3+2HCl=CaCl2+H2O+CO2↑ |
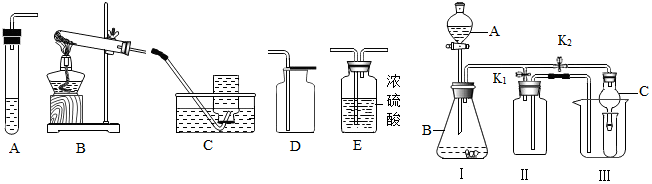
利用 I、Ⅱ装置可直接进行的实验是②(填序号).
①大理石与稀盐酸反应制取二氧化碳
②锌与稀硫酸反应制取氢气
(3)丙同学认为在不改变 I、Ⅱ、Ⅲ装置的仪器及位置的前提下,该装置可用于过氧化钠(Na2O2)固体与水
反应制取氧气,另一产物为氢氧化钠,则该反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑;她的改进措施是Ⅱ中把左边管加长,右边管变短.
(4)丁同学打开 K2、关闭 K1,利用 I、Ⅲ装置来验证生成的二氧化碳中含有水蒸气,此时 C 中盛放的物质是硫酸铜,可以观察到的现象是白色变蓝色.
(5)对用氯酸钾和二氧化锰的混合物制取 O2后的固体残渣(假定已完全反应)作如下回收处理:
①通过以下四步实验操作回收二氧化锰.正确操作的先后顺序是bcda(填写选项序号a. 烘干b. 溶解c.过滤d.洗涤
②用所得氯化钾晶体配制 50g 质量分数为 5%的氯化钾溶液,需要氯化钾的质量为2.5g
③过滤、蒸发时都需用到的仪器是C(填序号).
A. 酒精灯B. 烧杯C. 玻璃棒D.漏斗E.量筒
(6)小明用 6.5g 可能含有铜、铝、铁、镁中的一种或几种金属杂质的锌粉,跟足量的稀盐酸完全反应时,生成 0.2g 氢气,则此锌粉中一定含有的金属杂质是铜.
| A.化学与生活 | B.化学与安全 |
| ①用活性炭包可吸附汽车内的异味 ②用洗涤剂可以洗掉衣服和餐具上的油污 | ①炒菜时油锅着火可以用锅盖盖灭 ②在室内放一盆水能防止煤气中毒 |
| C.化学与资源 | D.化学与健康 |
| ①煤、石油、天然气都是可再生能源 ②我国试采可燃冰成功,为未来使用新能源提供可能 | ①烧烤食品营养丰富,可大量食用 ②每天食用适量蔬菜,以补充维生素 |
| A. | A | B. | B | C. | C | D. | D |
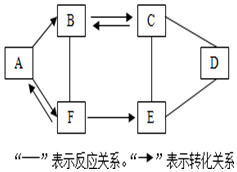 A~F为初中化学常见的六种物质,且都含有一种相同元素,它们相互间的关系如图所示.己知A、B、C、D、E是不同类别的物质,C俗称纯碱,F最常见的溶剂.(部分反应物、生成物及反应条件己略去)请回答:
A~F为初中化学常见的六种物质,且都含有一种相同元素,它们相互间的关系如图所示.己知A、B、C、D、E是不同类别的物质,C俗称纯碱,F最常见的溶剂.(部分反应物、生成物及反应条件己略去)请回答: