题目内容
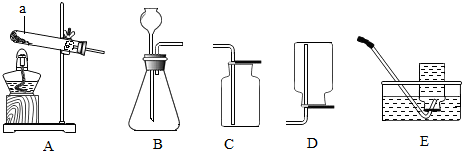
8.根据如图回答问题:
(1)装置图中标号仪器的名称:①试管,②集气瓶.
(2)实验室若用A装置制取氧气,反应的化学方程式是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(3)实验室制取二氧化碳的化学方程式是CaCO3+2HCl═CaCl2+CO2↑+H2O.若用G收集二氧化碳,二氧化碳应从a(选“a”或“b”)进,装置C与装置B相比,其主要优点是可以控制反应的发生或停止.
(4)工业上用碳酸钙在高温下分解来制取氧化钙和二氧化碳.
①若要制取5.6t氧化钙,需碳酸钙的质量是多少?(请写出计算过程)
②小华为测定某石灰石样品中碳酸钙的质量分数,取一定量的石灰石样品,将20g稀盐酸分4次加入样品中(样品中除碳酸钙外,其余成分不与盐酸反应,也不溶于水),充分反应后经过过滤、干燥等操作,最后称量,数据如下表:
| 稀盐酸的用量 | 剩余固体的质量 |
| 第一次加入5g | 1.5g |
| 第二次加入5g | 1.0g |
| 第三次加入5g | 0.5g |
| 第四次加入5g | 0.4g |
分析 试管是常用的反应容器,集气瓶是收集气体的仪器;制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.装置C的主要优点是:可以控制反应的发生或停止;有关的计算要准确.
解答 解:(1)试管是常用的反应容器,集气瓶是收集气体的仪器,故答案为:试管 集气瓶
(2)氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,配平即可;故答案为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
(3)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;若用G收集二氧化碳,二氧化碳应从长管进入,因为二氧化碳的密度比空气的密度大;装置C的主要优点是:可以控制反应的发生或停止;故答案为:CaCO3+2HCl═CaCl2+CO2↑+H2O a 可以控制反应的发生或停止
(4)①解:设需碳酸钙的质量为x.
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
100 56
x 5.6t $\frac{100}{56}=\frac{x}{5.6t}$ x=10t
答:需碳酸钙的质量为10t.
故答案为:10t;
②由表格信息可知:石灰石样品的质量是2g,杂质的质量是0.4g,因此碳酸钙的质量是1.6g;这种石灰石样品中碳酸钙的质量分数=$\frac{1.6g}{2g}×100%$=80%;若要制取5.6t氧化钙,理论上需要这种石灰石的质量=10t÷80%=12.5t;故答案为:80% 12.5t
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和有关的计算等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案| A. | 该气体的组成可能有2种情况 | B. | 该气体可能是CO和H2 | ||
| C. | 该气体不可能是纯净物 | D. | 该气体一定含有CH4 |
| 加热时间/min | 0 | t1 | t2 | t3 |
| 固体质量/g | 14.0 | 11.6 | 9.2 | 9.2 |
(2)计算反应前加入的二氧化锰的质量(写出计算过程)
(3)若将a克氯酸钾与X克二氧化锰混合,充分反应后得到b克固体,则X=b-$\frac{149}{245}$a.
 某化学兴趣小组设计了如下实验探究CO2的制取和性质:
某化学兴趣小组设计了如下实验探究CO2的制取和性质: