题目内容
17.为减少煤燃烧产生的二氧化硫对大气的污染,某发电厂向煤中加入适量的石灰石.若将7.2kg二氧化硫完全吸收,计算需要含90%碳酸钙的石灰石的质量.已知:2CaCO3+O2+2SO2$\frac{\underline{\;高温\;}}{\;}$2CaSO4+2CO2.
分析 根据反应的化学方程式和提供的数据可以进行相关方面的计算.
解答 解:设需要含90%碳酸钙的石灰石的质量为x,
2CaCO3+O2+2SO2$\frac{\underline{\;高温\;}}{\;}$2CaSO4+2CO2,
200 128
x×90% 7.2kg
$\frac{200}{x×90%}$=$\frac{128}{7.2kg}$,
x=12.5kg,
答:若将7.2kg二氧化硫完全吸收,计算需要含90%碳酸钙的石灰石的质量是12.5kg.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,同时考查了分析数据的能力,计算时要注意规范性和准确性.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
8.根据如图回答问题:

(1)装置图中标号仪器的名称:①试管,②集气瓶.
(2)实验室若用A装置制取氧气,反应的化学方程式是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(3)实验室制取二氧化碳的化学方程式是CaCO3+2HCl═CaCl2+CO2↑+H2O.若用G收集二氧化碳,二氧化碳应从a(选“a”或“b”)进,装置C与装置B相比,其主要优点是可以控制反应的发生或停止.
(4)工业上用碳酸钙在高温下分解来制取氧化钙和二氧化碳.
①若要制取5.6t氧化钙,需碳酸钙的质量是多少?(请写出计算过程)
②小华为测定某石灰石样品中碳酸钙的质量分数,取一定量的石灰石样品,将20g稀盐酸分4次加入样品中(样品中除碳酸钙外,其余成分不与盐酸反应,也不溶于水),充分反应后经过过滤、干燥等操作,最后称量,数据如下表:
这种石灰石样品中碳酸钙的质量分数为80%.若要制取5.6t氧化钙,理论上需要这种石灰石的质量是12.5t.

(1)装置图中标号仪器的名称:①试管,②集气瓶.
(2)实验室若用A装置制取氧气,反应的化学方程式是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(3)实验室制取二氧化碳的化学方程式是CaCO3+2HCl═CaCl2+CO2↑+H2O.若用G收集二氧化碳,二氧化碳应从a(选“a”或“b”)进,装置C与装置B相比,其主要优点是可以控制反应的发生或停止.
(4)工业上用碳酸钙在高温下分解来制取氧化钙和二氧化碳.
①若要制取5.6t氧化钙,需碳酸钙的质量是多少?(请写出计算过程)
②小华为测定某石灰石样品中碳酸钙的质量分数,取一定量的石灰石样品,将20g稀盐酸分4次加入样品中(样品中除碳酸钙外,其余成分不与盐酸反应,也不溶于水),充分反应后经过过滤、干燥等操作,最后称量,数据如下表:
| 稀盐酸的用量 | 剩余固体的质量 |
| 第一次加入5g | 1.5g |
| 第二次加入5g | 1.0g |
| 第三次加入5g | 0.5g |
| 第四次加入5g | 0.4g |
5.下列情况:①煤燃烧;②燃放鞭炮;③工业废气任意排放;④燃油汽车排放的尾气;⑤氢能源汽车排放的尾气.会引起空气污染的是( )
| A. | ①④⑤ | B. | ①②③④ | C. | ①②③⑤ | D. | ①②③④⑤ |
2.元素周期表中,氟元素的信息如图所示.下列解释不正确的是( )
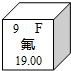

| A. | 原子序数是9 | B. | 氟是非金属元素 | ||
| C. | 质子数是19 | D. | 相对原子质量是19.00 |
6.红细胞的血红蛋白含有铁.这里的“铁”是指( )
| A. | 铁元素 | B. | 铁原子 | C. | 铁单质 | D. | 铁离子 |
7.下列有关碳和碳的氧化物的说法中不正确的是( )
| A. | 金刚石和石墨的结构中碳原子排列方式相同 | |
| B. | 工业中利用活性炭脱色以制白糖 | |
| C. | 室内放盆水不能防止一氧化碳中毒 | |
| D. | CO2可用于灭火,CO可用作燃料 |
