题目内容
一包白色粉末,由CuSO4、CaCO3、BaCl2、Na2SO4、NaOH中的两种或两种以上的物质混合而成,为探究其组成,进行如下实验:
(1)取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液;
(2)取实验(1)滤出的白色沉淀,向其中加入足量的盐酸,沉淀全部溶解,并产生无色气体
则下列有关说法正确的是( )
(1)取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液;
(2)取实验(1)滤出的白色沉淀,向其中加入足量的盐酸,沉淀全部溶解,并产生无色气体
则下列有关说法正确的是( )
| A、该白色粉末的成分中一定不含有CuSO4 |
| B、该白色粉末的成分中一定不含有NaOH |
| C、该白色粉末的组成有5种可能 |
| D、若向实验(1)得到的滤液中,通入二氧化碳,产生白色沉淀,则可推断原白色粉末由CaCO3和BaCl2组成 |
考点:物质的鉴别、推断,碱的化学性质,盐的化学性质
专题:混合物组成的推断题
分析:根据硫酸铜溶于水得到蓝色溶液,而本题中得到是无色的溶液,所以在混合物中一定不含硫酸铜,同时能形成白色沉淀的为碳酸钙,硫酸钠和氯化钡也可以反应生成白色沉淀,而白色沉淀能全部溶于稀硝酸,硫酸钠和氯化钡反应生成的硫酸钡不溶于稀盐酸,所以该沉淀为碳酸钙,即硫酸钠和氯化钡最多含有一种,可以据此分析判断并解答该题.
解答:解:A、把白色粉末溶解后得无色溶液,可知一定没有硫酸铜,因为硫酸铜溶于水会使溶液变蓝,故A说法正确;
B、题目中没有涉及氢氧化钠的验证,所以不能判断是否含有氢氧化钠,故B说法错误;
C、实验(1)中的白色固体可能是碳酸钙,也可能是硫酸钠与氯化钡反应后生成的硫酸钡沉淀,但是硫酸钡不溶于水而且不溶于酸,而题目中的白色沉淀全部溶于稀盐酸中,并产生无色气体,说明这种白色沉淀是碳酸钙;
由实验(2)可以分析出硫酸钠和氯化钡只能存在一种,或者都不存在,所以根据(1)和(2)的条件可以得出可能组合为:①CaCO3 BaCl2;②CaCO3 BaCl2 NaOH;③CaCO3 Na2SO4;④CaCO3 Na2SO4 NaOH;⑤CaCO3 NaOH 故有5种可能,故C说法正确;
D、二氧化碳不能和氯化钡反应,所以不能据此判断氯化钡的存在,若该操作中产生了白色沉淀,根据题给的物质可以知道,在该白色粉末中还含有氢氧化钠,氢氧化钠和二氧化碳反应生成了碳酸钠,而碳酸钠和氯化钡反应生成了白色沉淀,故D说法错误.
故选AC.
B、题目中没有涉及氢氧化钠的验证,所以不能判断是否含有氢氧化钠,故B说法错误;
C、实验(1)中的白色固体可能是碳酸钙,也可能是硫酸钠与氯化钡反应后生成的硫酸钡沉淀,但是硫酸钡不溶于水而且不溶于酸,而题目中的白色沉淀全部溶于稀盐酸中,并产生无色气体,说明这种白色沉淀是碳酸钙;
由实验(2)可以分析出硫酸钠和氯化钡只能存在一种,或者都不存在,所以根据(1)和(2)的条件可以得出可能组合为:①CaCO3 BaCl2;②CaCO3 BaCl2 NaOH;③CaCO3 Na2SO4;④CaCO3 Na2SO4 NaOH;⑤CaCO3 NaOH 故有5种可能,故C说法正确;
D、二氧化碳不能和氯化钡反应,所以不能据此判断氯化钡的存在,若该操作中产生了白色沉淀,根据题给的物质可以知道,在该白色粉末中还含有氢氧化钠,氢氧化钠和二氧化碳反应生成了碳酸钠,而碳酸钠和氯化钡反应生成了白色沉淀,故D说法错误.
故选AC.
点评:本题属于文字叙述型推断题,在给定的物质范围和实验现象,来推出混合物中一定存在、一定不存在和可能存在的是什么物质;解答时以文字信息为序,寻找并抓住“题眼”,逐步分析“筛选”最终得出答案即可.

练习册系列答案
相关题目
下列变化中,属于化学变化的是( )
| A、酒精燃烧 | B、滴水成冰 |
| C、玻璃破碎 | D、西瓜榨汁 |
法国化学家肖万、美国化学家格拉布斯和施罗克在有机化学领域研究中作出了重要贡献,其研究成果可以简单描述为如下的反应(R1~R8为H-、CH3-、C2H5-…等).
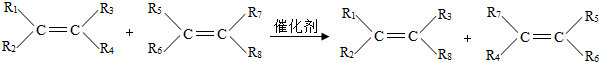
上述反应类似于无机反应中的( )

上述反应类似于无机反应中的( )
| A、置换反应 | B、分解反应 |
| C、化合反应 | D、复分解反应 |
某同学的有关实验操作和实验现象描述如下,你认为正确的是( )
| A、将pH试纸伸入NaCl溶液中测定其pH=7 |
| B、过滤时用蒸馏水洗涤滤纸上的不溶性物质,以除去其表面的可溶性物质 |
| C、用熟石灰与某化肥一起研磨,未闻到刺激性气味,则该化肥不可能是氮肥 |
| D、对浓硫酸进行稀释时,应将水沿烧杯壁慢慢注入浓硫酸中,并用玻璃棒不断地搅拌 |


 如图是某胃药标签上的部分内容,某中学化学兴趣小组欲测定该药品中碳酸氢钠(NaHCO3)的质量分数,取10片该药品研碎放入烧杯中,再向烧杯中滴加稀盐酸至恰好完全反应(杂质不溶于水,也不参加反应.反应的化学方程式为
如图是某胃药标签上的部分内容,某中学化学兴趣小组欲测定该药品中碳酸氢钠(NaHCO3)的质量分数,取10片该药品研碎放入烧杯中,再向烧杯中滴加稀盐酸至恰好完全反应(杂质不溶于水,也不参加反应.反应的化学方程式为