题目内容
根据下列有关实验回答下列问题:

(1)实验一是分解H2O2中MnO2作用的探究.步骤①的作用是 ;步骤③反应结束后向试管中再加入5%H2O2溶液,观察到的现象是 ,再把试管液体蒸干,全部取出称量,质量 (填“大于”、“小于”或“等于”)0.5g.
(2)实验二是可燃物燃烧条件的探究,其中能发生燃烧的是 (填“a“、”b“或”c),燃烧一段时间后熄灭的可能原因是 (选填序号).
A.温度低于着火点 B.氧气消耗完 C.白磷消耗完.

(1)实验一是分解H2O2中MnO2作用的探究.步骤①的作用是
(2)实验二是可燃物燃烧条件的探究,其中能发生燃烧的是
A.温度低于着火点 B.氧气消耗完 C.白磷消耗完.
考点:催化剂的特点与催化作用,燃烧与燃烧的条件
专题:实验性简答题
分析:(1)根据二氧化锰对过氧化氢的分解有催化作用回答;根据催化剂的定义和特点回答⑥结果;根据催化剂的定义和特点回答;根据对比实验的探究方法回答;
(2)根据可燃物的燃烧条件分析.
(2)根据可燃物的燃烧条件分析.
解答:解:催化剂的特点是“一变,两不变”,即反应速率变,质量和化学性质不变;
(1)为了看氧化铜是否能改变反应的速率,要通过加入二氧化锰与不加二氧化锰的现象进行对比,才能得出科学合理的结论;
二氧化锰对过氧化氢的分解有催化作用,能加快其分解速率生成氧气的速率,故现象是有气泡,带火星的木条复燃;催化剂的特点是“一变,两不变”,反应前后其质量不变,所以二氧化锰的质量仍为0.5g;催化剂的特点是“一变,两不变”,其中反应速率改变,这里是加快,所以现象是溶液中有气泡放出,带火星的木条复燃;
(2)a处的白磷温度达到着火点,与空气中的氧气接触,满足燃烧的条件;燃烧一段时间后熄灭的可能原因是氧气消耗完,白磷烧尽;
故答案为:
(1)作对照 有气泡迅速放出,带火星木条复燃 等于
通电
(2)a BC(有错、漏不得分)
(1)为了看氧化铜是否能改变反应的速率,要通过加入二氧化锰与不加二氧化锰的现象进行对比,才能得出科学合理的结论;
二氧化锰对过氧化氢的分解有催化作用,能加快其分解速率生成氧气的速率,故现象是有气泡,带火星的木条复燃;催化剂的特点是“一变,两不变”,反应前后其质量不变,所以二氧化锰的质量仍为0.5g;催化剂的特点是“一变,两不变”,其中反应速率改变,这里是加快,所以现象是溶液中有气泡放出,带火星的木条复燃;
(2)a处的白磷温度达到着火点,与空气中的氧气接触,满足燃烧的条件;燃烧一段时间后熄灭的可能原因是氧气消耗完,白磷烧尽;
故答案为:
(1)作对照 有气泡迅速放出,带火星木条复燃 等于
通电
(2)a BC(有错、漏不得分)
点评:催化剂、催化作用是初中重要基本概念之一,是考查的重点和热点,主要考查对催化剂、催化作用概念的理解,对催化效率影响因素的探究等.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
下列物质的俗名与化学式相对应正确的是( )
| A、天然气:CO |
| B、烧碱:Na2CO3 |
| C、火碱:KOH |
| D、熟石灰:Ca(OH)2 |
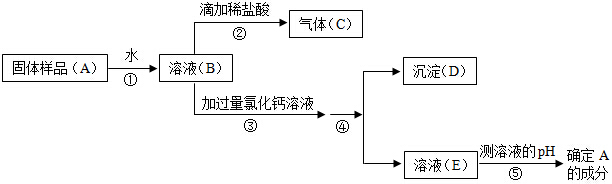
一包白色粉末,由CuSO4、CaCO3、BaCl2、Na2SO4、NaOH中的两种或两种以上的物质混合而成,为探究其组成,进行如下实验:
(1)取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液;
(2)取实验(1)滤出的白色沉淀,向其中加入足量的盐酸,沉淀全部溶解,并产生无色气体
则下列有关说法正确的是( )
(1)取少量白色粉末,向其中加入足量的水,充分搅拌后过滤,得到白色沉淀和无色滤液;
(2)取实验(1)滤出的白色沉淀,向其中加入足量的盐酸,沉淀全部溶解,并产生无色气体
则下列有关说法正确的是( )
| A、该白色粉末的成分中一定不含有CuSO4 |
| B、该白色粉末的成分中一定不含有NaOH |
| C、该白色粉末的组成有5种可能 |
| D、若向实验(1)得到的滤液中,通入二氧化碳,产生白色沉淀,则可推断原白色粉末由CaCO3和BaCl2组成 |