题目内容
某学习小组围绕“气体的实验室制取”进行研讨,请你参与完成下面的问题.
(1)图1中①装置制取气体的适用条件是 .
(2)图1中③装置相比图②装置的主要优点是 .
(3)实验室不宜用镁来代替锌与稀H2SO4反应制取H2,主要原因是 .
(4)实验室若用图1中④装置收集NH3时,气体应从 端通入.(填字母)
(5)为了测定铜元素的相对原子质量Ar(Cu),某同学以氢气还原氧化铜的反应设计了一组实验(见图2).
图2中第一个装有碱石灰的U形管的作用是 .若测得反应前氧化铜的质量为a g,实验完成后第二装有碱石灰的U形管增加的质量为b g,则Ar(Cu)= .(用a、b表示)
(6)请利用单孔橡胶塞、玻璃导管、胶皮管、试管、集气瓶和玻璃片,设计一套制取CO2的实验装置,并将该实验装置的简图画出来.

(1)图1中①装置制取气体的适用条件是
(2)图1中③装置相比图②装置的主要优点是
(3)实验室不宜用镁来代替锌与稀H2SO4反应制取H2,主要原因是
(4)实验室若用图1中④装置收集NH3时,气体应从
(5)为了测定铜元素的相对原子质量Ar(Cu),某同学以氢气还原氧化铜的反应设计了一组实验(见图2).
图2中第一个装有碱石灰的U形管的作用是
(6)请利用单孔橡胶塞、玻璃导管、胶皮管、试管、集气瓶和玻璃片,设计一套制取CO2的实验装置,并将该实验装置的简图画出来.
考点:常用气体的发生装置和收集装置与选取方法,实验室制取氧气的反应原理,二氧化碳的实验室制法,氢气的制取和检验,氢气的化学性质与燃烧实验
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1))根据发生装置的选择条件即可.
(2)根据发生装置和收集装置的选择条件即可.
(3)镁比锌活泼,与稀硫酸反应剧烈得多,不利于收集氢气;
(4)根据氨气的密度及溶解性选择收集方法;
(5)通入硬试管中的氢气要干燥,第一个装有碱石灰的U形管的作用是除去氢气中的水分;由装置图与实验原理可知,第二个装有碱石灰的U形管的作用是用于吸收反应产生的水,根据水的质量测定铜元素的相对原子质量Ar(Cu),;
(6)根据题意分析制图.
(2)根据发生装置和收集装置的选择条件即可.
(3)镁比锌活泼,与稀硫酸反应剧烈得多,不利于收集氢气;
(4)根据氨气的密度及溶解性选择收集方法;
(5)通入硬试管中的氢气要干燥,第一个装有碱石灰的U形管的作用是除去氢气中的水分;由装置图与实验原理可知,第二个装有碱石灰的U形管的作用是用于吸收反应产生的水,根据水的质量测定铜元素的相对原子质量Ar(Cu),;
(6)根据题意分析制图.
解答:解:
(1)初中所学发生装置主要分两种,即固体加热型、固体和液体不加热型.A装置属于固体和固体加热装置,反应物是固体和固体,反应条件是加热,故答案为:反应物是固体且需加热.
(2)实验室用大理石和稀盐酸制取二氧化碳,发生装置属于固体和液体不加热制气体;②和③相比,③装置中导管多了一个开关,一旦开关关闭,随着气体的增多,迫使液体和多孔隔板上的固体分离,导致反应停止,故答案为:可随时控制反应的发生和停止;
(3)实验室不宜用镁来代替锌与稀H2SO4反应制取H2,主要原因是:镁比锌活泼,与稀硫酸反应剧烈得多,不利于收集氢气;
(4)因为氨气易溶于水,密度比空气小,故采用向下排空气法收集,故从短管(b)通入,把空气从长管排出;
(5))通入硬试管中的氢气要干燥,第一个装有碱石灰的U形管的作用是除去氢气中的水分;依据H2+CuO
Cu+H2O;
氧化铜的质量为ag,反应后生成水的质量为bg,令铜的相对原子质量为x,则(x+16):18=ag:bg,解得x=
.
(6)请利用单孔橡胶塞、玻璃导管、胶皮管、试管、集气瓶和玻璃片,设计一套制取CO2的实验装置,并将该实验装置的简图画出来(如答案图所示).

故本题答案为:(1)反应物是固体且需加热;
(2)可随时控制反应的发生和停止;
(3)镁比锌活泼,与稀硫酸反应剧烈得多,不利于收集氢气;
(4)b;
(5)
;
(6)
(1)初中所学发生装置主要分两种,即固体加热型、固体和液体不加热型.A装置属于固体和固体加热装置,反应物是固体和固体,反应条件是加热,故答案为:反应物是固体且需加热.
(2)实验室用大理石和稀盐酸制取二氧化碳,发生装置属于固体和液体不加热制气体;②和③相比,③装置中导管多了一个开关,一旦开关关闭,随着气体的增多,迫使液体和多孔隔板上的固体分离,导致反应停止,故答案为:可随时控制反应的发生和停止;
(3)实验室不宜用镁来代替锌与稀H2SO4反应制取H2,主要原因是:镁比锌活泼,与稀硫酸反应剧烈得多,不利于收集氢气;
(4)因为氨气易溶于水,密度比空气小,故采用向下排空气法收集,故从短管(b)通入,把空气从长管排出;
(5))通入硬试管中的氢气要干燥,第一个装有碱石灰的U形管的作用是除去氢气中的水分;依据H2+CuO
| ||
氧化铜的质量为ag,反应后生成水的质量为bg,令铜的相对原子质量为x,则(x+16):18=ag:bg,解得x=
| 18a-16b |
| b |
(6)请利用单孔橡胶塞、玻璃导管、胶皮管、试管、集气瓶和玻璃片,设计一套制取CO2的实验装置,并将该实验装置的简图画出来(如答案图所示).

故本题答案为:(1)反应物是固体且需加热;
(2)可随时控制反应的发生和停止;
(3)镁比锌活泼,与稀硫酸反应剧烈得多,不利于收集氢气;
(4)b;
(5)
| 18a-16b |
| b |
(6)

点评:此题重在考查同学们对常用化学仪器的了解和识记情况,只有很好的认识它们,做实验才能得心应手.属于扩展性问题,重在考查根据物质的反应物和反应条件选取装置.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
一种元素与另一种元素的区别在于( )
| A、相对原子质量不同 |
| B、核电荷数不同 |
| C、中子数不同 |
| D、最外层电子数不同 |
 法国化学家拉瓦锡用定量的方法研究了空气的成分.整个实验过程如图所示:
法国化学家拉瓦锡用定量的方法研究了空气的成分.整个实验过程如图所示: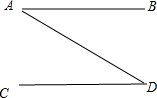 如图所示,A、B、C、D分别为下列物质中的某一种:二氧化碳、火碱、熟石灰和硫酸铜,图中直线相连的两种物质或其溶液能相互发生反应.
如图所示,A、B、C、D分别为下列物质中的某一种:二氧化碳、火碱、熟石灰和硫酸铜,图中直线相连的两种物质或其溶液能相互发生反应.