题目内容
16.选择适当物质的序号填空.A.二氧化碳 B.硝酸钾 C.明矾 D.氮气 E.氧化钙 F.石灰石
(1)可用于人工降雨的是A; (2)农业上可作复合肥的是B;
(3)可用于净水的是C; (4)常用于保护蔬菜瓜果的气体是D;
(5)用于作食品干燥剂的E; (6)可用作建筑材料的是F.
分析 二氧化碳的固体干冰,升华时吸收大量的热,可以用于人工降雨和做制冷剂;硝酸钾中的营养元素是钾元素和氮元素,因此是属于复合肥;明矾起净水作用,是常用的净水剂;氮气的化学性质稳定,常用作保护气;氧化钙能和水反应,可做干燥剂;石灰石是常用的建筑材料.
解答 解:(1)二氧化碳的固体干冰,升华时吸收大量的热,可以用于人工降雨和做制冷剂,故答案为:A;
(2)硝酸钾中的营养元素是钾元素和氮元素,因此是属于复合肥,故答案为:B
(3)明矾起净水作用,是常用的净水剂,故答案为:C;
(4)氮气的化学性质稳定,常用作保护气,故答案为:D
(5)氧化钙能和水反应,用于作食品干燥剂,故答案为:E;
(6)石灰石是常用的建筑材料,故答案为:F.
点评 物质的结构决定物质的性质,物质的性质决定物质的用途,要善于根据物质的性质来确定物质的用途.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.下列物质的用途主要由化学性质决定的是( )
| A. | 活性炭用作吸附剂 | B. | 干冰用于人工降雨 | ||
| C. | 肥皂水用于区别硬水和软水 | D. | 液态氮作制冷剂 |
7.下列关于镁原子、镁离子叙述正确的是( )
| A. | 它们都显电性 | |
| B. | 它们原子核外电子数目相等 | |
| C. | 它们属于同种元素 | |
| D. | 镁离子是镁原子得到2个电子形成的 |
1.分类是学习化学的一种重要科学方法.下列物质分类正确的是( )
| A. | 常见的活泼金属:镁、锌、铜 | |
| B. | 常见的营养素:糖类、蛋白质、无机盐 | |
| C. | 常见的易燃物:汽油、酒精、浓硫酸 | |
| D. | 常见的氧化物:水、氧化铜、熟石灰 |
8.氮化铝(AlN)是新型的电子绝缘基片材料,用于大型和超大型集成电路中.在高温下氮气、碳和三氧化二铝反应可以生成氮化铝微晶粉体和一氧化碳,用此方法制得的氮化铝中含有少量杂质碳和氧化铝.某校化学兴趣小组利用上述反应原理制取并测定所得样品中氮化铝的质量分数.
【查阅资料】
(1)Al2O3+2NaOH=2NaAlO2+H2O;
(2)AlN+NaOH+H2O=NaAlO2+NH3↑;
(3)氨气易与酸反应.
【设计实验】
实验一:制取氮化铝样品
实验二:测定所制氮化铝样品中氮化铝的质量分数
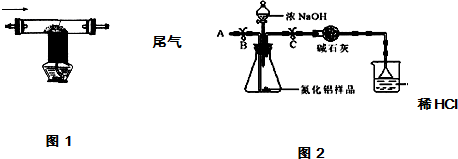
①按图2组装仪器,将9.1g氮化铝样品放入锥形瓶中,在分液漏斗中加入一定量的浓NaOH溶液
②称得盛有稀盐酸的烧杯和漏斗的总质量为200g
③打开止水夹C,从分液漏斗向锥形瓶中滴入浓NaOH溶液,直到不再产生气体为止
④打开止水夹B,从导管A处缓缓鼓入一定量的空气
⑤再次称量盛有稀盐酸的烧杯和漏斗的质量和为203.4g
⑥重复实验④⑤步骤后称得盛有稀盐酸的烧杯和漏斗的总质量仍为203.4g
【实验讨论】
(1)步骤①加入样品前还应检查装置气密性.
(2)装有碱石灰的干燥管作用是除去气体中的水;装置中使用漏斗的目的是防止液体倒吸.
(3)图2烧杯中稀盐酸不能换成浓盐酸的理由是浓盐酸具有挥发性;
(4)步骤④的目的是使反应产生的氨气充分吸收.
【实验结论】
所制氮化铝样品中氮化铝的质量分数为90%
【事故处理】
实验中,小明不小心将盛有约50mL的浓NaOH溶液打翻在桌面上.这时他应该采取的措施是:立即用稀醋酸中和,然后用水冲洗,再用抹布擦干.
【拓展探究】
(1)实验后剩余的浓NaOH溶液不能(能或不能)放回原试剂瓶,写出NaOH溶液露置在空气中发生的化学反应方程式2NaOH+CO2═Na2CO3+H2O.
(2)本着节约药品的原则,同时又要确保实验顺利获得成功.则实验二中至少应准备40%浓NaOH溶液20g.
【查阅资料】
(1)Al2O3+2NaOH=2NaAlO2+H2O;
(2)AlN+NaOH+H2O=NaAlO2+NH3↑;
(3)氨气易与酸反应.
【设计实验】
实验一:制取氮化铝样品
| 实验步骤 | 相关化学反应方程式 |
| 1除去空气中粉尘、二氧化碳、干燥后,再除去氧气. | 除去氧气的化学反应方程式为2Cu+O2$\frac{\underline{\;高温\;}}{\;}$2CuO; |
| 2用上述制得的氮气通入装有碳和三氧化二铝硬质玻璃管中高温制取氮化铝样品(如图1). | 装置中发生化学反应的化学方程式为 N2+3C+Al2O3 $\frac{\underline{\;高温\;}}{\;}$2AlN+3CO. |
①按图2组装仪器,将9.1g氮化铝样品放入锥形瓶中,在分液漏斗中加入一定量的浓NaOH溶液
②称得盛有稀盐酸的烧杯和漏斗的总质量为200g
③打开止水夹C,从分液漏斗向锥形瓶中滴入浓NaOH溶液,直到不再产生气体为止
④打开止水夹B,从导管A处缓缓鼓入一定量的空气
⑤再次称量盛有稀盐酸的烧杯和漏斗的质量和为203.4g

⑥重复实验④⑤步骤后称得盛有稀盐酸的烧杯和漏斗的总质量仍为203.4g
【实验讨论】
(1)步骤①加入样品前还应检查装置气密性.
(2)装有碱石灰的干燥管作用是除去气体中的水;装置中使用漏斗的目的是防止液体倒吸.
(3)图2烧杯中稀盐酸不能换成浓盐酸的理由是浓盐酸具有挥发性;
(4)步骤④的目的是使反应产生的氨气充分吸收.
【实验结论】
所制氮化铝样品中氮化铝的质量分数为90%
【事故处理】
实验中,小明不小心将盛有约50mL的浓NaOH溶液打翻在桌面上.这时他应该采取的措施是:立即用稀醋酸中和,然后用水冲洗,再用抹布擦干.
【拓展探究】
(1)实验后剩余的浓NaOH溶液不能(能或不能)放回原试剂瓶,写出NaOH溶液露置在空气中发生的化学反应方程式2NaOH+CO2═Na2CO3+H2O.
(2)本着节约药品的原则,同时又要确保实验顺利获得成功.则实验二中至少应准备40%浓NaOH溶液20g.
5.Mn03中锰元素的化合价为( )
| A. | 0 | B. | +2 | C. | +4 | D. | +6 |