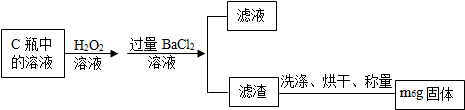
题目内容
11.现在有Fe、C、O、H、Cl、Na六种元素,从中选择适当的元素完成下列填空(1)写出符合下列要求的化学式:一种金属单质Fe或Na,一种金属氧化物Fe2O3,一种酸HCl,
一种难溶性碱Fe(OH)3,一种碳酸盐Na2CO3.
(2)写出符合下列要求的化学方程式:
酸+金属:Fe+H2SO4=FeSO4+H2↑,
酸+金属氧化物:6HCl+Fe2O3═2FeCl3+3H2O,
酸+碱:NaOH+HCl=NaCl+H2O,
酸+碳酸盐:Na2CO3+2HCl=2NaCl+H2O+CO2↑,
碱+非金属氧化物:CO2+2NaOH=Na2CO3+H2O,
碱+盐:3NaOH+FeCl3=Fe(OH)3↓+3NaCl.
分析 (1)首先根据题意确定物质的化学名称,然后根据题目所提供的元素、物质分类的知识、书写化学式的方法和步骤写出物质的化学式即可;
(2)首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
解答 解:(1)Fe、C、O、H、Cl、Na六种元素可组成的物质:
铁和钠属于金属单质;氧化铁、四氧化三铁、氧化钠属于金属氧化物;碳酸和盐酸属于酸;氢氧化铁属于难溶性碱;碳酸钠属于碳酸盐;故填:Fe或Na;Fe2O3;HCl;Fe(OH)3;Na2CO3;
(2)铁是金属,与酸--稀硫酸反应生成硫酸亚铁和氢气;故填:Fe+H2SO4=FeSO4+H2↑;
氧化铁属于金属氧化物,盐酸属于酸,二者反应生成氯化铁和水,故填:6HCl+Fe2O3═2FeCl3+3H2O;
氢氧化钠属于碱、盐酸属于酸,二者发生中和反应生成氯化钠和水,故填:NaOH+HCl=NaCl+H2O;
盐酸属于酸,碳酸钠属于碳酸盐,二者反应生成氯化钠、水和二氧化碳,故填:Na2CO3+2HCl=2NaCl+H2O+CO2↑;
氢氧化钠属于碱,二氧化碳属于非金属氧化物,二者反应生成碳酸钠和水,故填:CO2+2NaOH=Na2CO3+H2O;
氢氧化钠属于碱,氯化铁属于盐,二者发生复分解反应生成氢氧化铁沉淀和氯化钠,故填:3NaOH+FeCl3=Fe(OH)3↓+3NaCl.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
相关题目
2.下列关于元素的说法中正确的是( )
| A. | 具有相同核电荷数(即核内质子数)的一类原子的总称 | |
| B. | 是相对原子质量相同的一类原子的总称 | |
| C. | 是具有相同电子数的一类原子的总称 | |
| D. | 是具有相同中子数的一类原子的总称 |
19.钢铁工业是国家工业的基础. 某兴趣小组在实验室中模拟炼铁化学原理的实验,对固体产物成分等进行探究.
[设计实验]
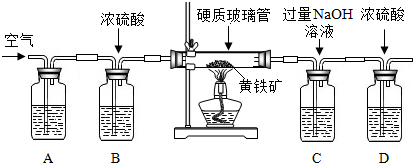
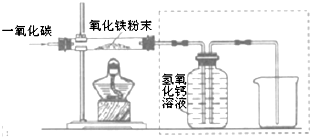
用一氧化碳还原纯净的氧化铁粉末,实验装置如图.
[进行实验]
该小组按上述实验设计,在一定温度下进行了实验,测得下列数据:
①反应前玻璃管和内盛氧化铁粉末的总质量66.0g(玻璃管的质量为60.0g)
②反应后玻璃管和内盛黑色固体的总质量65.8g(冷却到室温称量)
[分析与讨论]
本实验中,玻璃管内固体粉末由红色全部变为黑色.小明同学认为该黑色固体全部是铁,但小华同学提出了质疑,于是大家提出查阅资料.
[查阅资料]
①一氧化碳还原氧化铁的固体产物的成分与反应温度、反应时间等因素有关.
②一氧化碳还原氧化铁的实验过程中固体产物可能有四氧化三铁、氧化亚铁、铁.
[实验与猜想]
①该小组同学将反应后的黑色固体研磨后,再用磁铁吸引,发现黑色固体粉末全部能被吸引,则该黑色固体粉末中不可能含有氧化铁和氧化亚铁.
②进行猜想:黑色固体粉末可能
a.全部为铁 b.全部是四氧化三铁 c铁与四氧化三铁的混合物.
[得出结论]
通过实验中获得的数据进行计算,得出黑色固体粉末为(写名称)四氧化三铁.
[反思与评价]
①一氧化碳还原氧化铁的实验中,若要得到铁可适当提高反应温度和延长反应时间.
②实验装置图中采用虚线框内的装置,其作用有A、B.
A.收集一氧化碳 B.吸收二氧化碳 C.检验二氧化碳.
[设计实验]
用一氧化碳还原纯净的氧化铁粉末,实验装置如图.

[进行实验]
该小组按上述实验设计,在一定温度下进行了实验,测得下列数据:
①反应前玻璃管和内盛氧化铁粉末的总质量66.0g(玻璃管的质量为60.0g)
②反应后玻璃管和内盛黑色固体的总质量65.8g(冷却到室温称量)
| 物质 性质 | 四氧化三铁 | 氧化亚铁 | 氧化铁 | 铁粉 |
| 颜色 | 黑色 | 黑色 | 红色 | 黑色 |
| 能否被磁铁吸引 | 能 | 不能 | 不能 | 能 |
本实验中,玻璃管内固体粉末由红色全部变为黑色.小明同学认为该黑色固体全部是铁,但小华同学提出了质疑,于是大家提出查阅资料.
[查阅资料]
①一氧化碳还原氧化铁的固体产物的成分与反应温度、反应时间等因素有关.
②一氧化碳还原氧化铁的实验过程中固体产物可能有四氧化三铁、氧化亚铁、铁.
[实验与猜想]
①该小组同学将反应后的黑色固体研磨后,再用磁铁吸引,发现黑色固体粉末全部能被吸引,则该黑色固体粉末中不可能含有氧化铁和氧化亚铁.
②进行猜想:黑色固体粉末可能
a.全部为铁 b.全部是四氧化三铁 c铁与四氧化三铁的混合物.
[得出结论]
通过实验中获得的数据进行计算,得出黑色固体粉末为(写名称)四氧化三铁.
[反思与评价]
①一氧化碳还原氧化铁的实验中,若要得到铁可适当提高反应温度和延长反应时间.
②实验装置图中采用虚线框内的装置,其作用有A、B.
A.收集一氧化碳 B.吸收二氧化碳 C.检验二氧化碳.
3.Fe2O3、CuO的混合粉末10g,高温下与足量H2充分反应后,得到固体的质量可能为( )
| A. | 7.2g | B. | 5.8g | C. | 4.4g | D. | 9.5 g |
1.增加沈阳的绿化面积,目的是有助于减少空气中哪种成分的含量( )
| A. | 氧气 | B. | 二氧化碳 | C. | 氮气 | D. | 稀有气体 |
 在“侯式联合制碱法”的工艺流程中,最后一步是用加热碳酸氢钠的方法来制取纯碱.某纯碱生产厂制得的样品Na2CO3中混有少量NaHCO3.为了测定样品中Na2CO3的质量分数,取100g混合物加热(2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,Na2CO3受热不分解),反应过程中生成二氧化碳气体的质量与反应时间的关系如图所示.
在“侯式联合制碱法”的工艺流程中,最后一步是用加热碳酸氢钠的方法来制取纯碱.某纯碱生产厂制得的样品Na2CO3中混有少量NaHCO3.为了测定样品中Na2CO3的质量分数,取100g混合物加热(2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,Na2CO3受热不分解),反应过程中生成二氧化碳气体的质量与反应时间的关系如图所示.