题目内容
9.甲和乙在一定条件下反应生成丙和丁,结合微观示意图分析,结论正确的是( )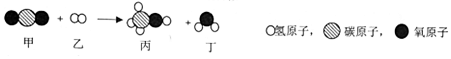
| A. | 反应过程中只有丁属于氧化物 | |
| B. | 发生反应的甲和乙的质量比为22:1 | |
| C. | 可用于减少温室气体的排放 | |
| D. | 反应前后,原子的种数不变,数目改变 |
分析 观察微观示意图,分析反应物、生成物的化学式,根据反应写出反应的化学方程式.根据化学式、方程式的意义计算、分析、判断有关的问题.
解答 解:由反应的微观示意图可知,该反应是二氧化碳和氢气在一定条件下反应生成了甲醇和水,反应的方程式是:CO2+3H2$\frac{\underline{\;一定条件\;}}{\;}$CH3OH+H2O.
A、由上述方程式可知,甲物质是二氧化碳,丁物质是水,都属于氧化物,故A错误;
B、由反应的方程式可知,发生反应的甲和乙的质量比为44:(3×1×2)=22:3.故B错误;
C、由上述方程式可知,该反应中二氧化碳作为反应物,因此可以减少二氧化碳的排放.故C正确;
D、由上述方程式可知,反应前后,原子的种数和数目都不变,故D错误.
故选:C.
点评 解答本题比较简便的方法是根据微观示意图写出反应的化学方程式,根据方程式的意义分析解答.

练习册系列答案
相关题目
20.下列实验操作正确的是( )
| A. |  过滤 | B. |  测定溶液pH | C. |  稀释浓硫酸 | D. |  熄灭酒精灯 |
14.能源危机和全球变暖是21世纪人类面临的两大严峻问题.近日,中国科学技术大学谢毅教授课题组在四氧化三钴(Co3O4)超薄二维片状材料电催化CO2还原成化学燃料甲酸(HCOOH)的研究方面取得进展,此法不仅能够减少CO2的排放,还能够解决能源危机问题.下列说法正确的是( )
| A. | Co3O4和HCOOH都属于氧化物 | |
| B. | Co3O4中Co元素为+3价 | |
| C. | HCOOH由1个碳原子、2个氧原子、2个氢原子构成 | |
| D. | HCOOH中氧元素质量分数最大 |
1.建立微观和宏观之间的联系是一种科学的思维方式,下列叙述错误的是( )
| A. | 金刚石和石墨的物理性质差异较大,是因为构成它们的微粒种类不同 | |
| B. | 冰和干冰的化学性质存在差异,因为构成它们的微粒种类不同 | |
| C. | 酸碱中和反应都生成水,其实质是H+与OH-结合生成了H2O | |
| D. | NaOH和KOH都具有碱性,其原因是在水中均能解离出OH- |
 A、B、C、D为初中化学常见的物质,它们之间存在一定的关系,请根据下列叙述回答问题.“-”表示两端的物质能反应,“→”表示物质间存在转化关系.(部分生成物和反应条件已略去).
A、B、C、D为初中化学常见的物质,它们之间存在一定的关系,请根据下列叙述回答问题.“-”表示两端的物质能反应,“→”表示物质间存在转化关系.(部分生成物和反应条件已略去).