题目内容
6.用所学的知识填空.(每小题2分)(1)SO2与SO3中所含氧元素的质量相等,则SO2与SO3的质量比为6:5.
(2)相同质量的SO2与SO3中,则SO2与SO3的分子个数比为5:4.
(3)某铁的氧化物中,铁元素与氧元素的质量比为7:3,则它的化学式是Fe2O3.
分析 (1)要使SO2和SO3含有相同质量的氧元素,则氧原子的个数应相等,3SO2和2SO3中氧原子个数相等,据此进行分析判断;
(2)根据质量相同的SO2和SO3,它们的分子数之比等于质量除以相对分子质量之比来分析;
(3)设铁的氧化物中Fe、O的原子个数为x、y,然后利用元素的质量比为7:3来计算,求出x与y的比,得到化学式.
解答 解:(1)要使SO2和SO3含有相同质量的氧元素,则氧原子的个数应相等,3SO2和2SO3中氧原子个数相等,则SO2和SO3的质量比(3×64):(2×80)=6:5.故答案为:6:5;
(2)设相同的质量为m.质量相同的SO2和SO3,它们的分子数之比为$\frac{\frac{m}{64}}{\frac{m}{80}}$=$\frac{5}{4}$;故填:5:4;
(3)设铁的氧化物中Fe、O的原子个数为x、y,
则由Fe、O元素的质量比为7:3,得:
$\frac{56x}{16y}=\frac{7}{3}$
$\frac{x}{y}=\frac{2}{3}$
则铁的氧化物的化学式为:Fe2O3.
故答案为:Fe2O3.
点评 本题主要考查学生运用化学式进行计算的能力.学生需根据题意的要求,运用假设法,才能正确解答.

练习册系列答案
相关题目
14.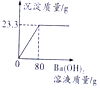 用氢氧化钡溶液测定某种氮肥中硫酸铵的质量分数(杂质溶于水,但不参加反应),实验如下:称取该氮肥20g加水完全溶解,向该溶液中不断滴入氢氧化钡溶液,生成气体及沉淀质量与加入氢氧化钡溶液的质量关系如表所示:
用氢氧化钡溶液测定某种氮肥中硫酸铵的质量分数(杂质溶于水,但不参加反应),实验如下:称取该氮肥20g加水完全溶解,向该溶液中不断滴入氢氧化钡溶液,生成气体及沉淀质量与加入氢氧化钡溶液的质量关系如表所示:
试分析并计算:【已知:(NH4)2SO4+Ba(OH)2═BaSO4↓+2NH3↑+2H2O】
(1)硫酸铵中氮元素与氢元素的质量比为7:2.
(2)表格中m的值为1.70.
(3)该氮肥中硫酸铵的质量分数.
 用氢氧化钡溶液测定某种氮肥中硫酸铵的质量分数(杂质溶于水,但不参加反应),实验如下:称取该氮肥20g加水完全溶解,向该溶液中不断滴入氢氧化钡溶液,生成气体及沉淀质量与加入氢氧化钡溶液的质量关系如表所示:
用氢氧化钡溶液测定某种氮肥中硫酸铵的质量分数(杂质溶于水,但不参加反应),实验如下:称取该氮肥20g加水完全溶解,向该溶液中不断滴入氢氧化钡溶液,生成气体及沉淀质量与加入氢氧化钡溶液的质量关系如表所示:| 实验次序 | 1 | 2 | 3 |
| 滴入Ba(OH)2溶液的质量/g | 20 | 40 | 60 |
| 生成气体的质量/g | 0.85 | m | 2.55 |
(1)硫酸铵中氮元素与氢元素的质量比为7:2.
(2)表格中m的值为1.70.
(3)该氮肥中硫酸铵的质量分数.
1.下列图象分别与选项中的操作相对应,其中合理的是( )
| A. |  向一定量稀氢氧化钾溶液中滴入水 | |
| B. |  向一定量氯化亚铁溶液中加入过量锌粉 | |
| C. |  向浑浊的石灰水中滴加浓硫酸 | |
| D. |  向少量硫酸和硫酸铁混合溶液中边滴氢氧化钠溶液边振荡 |
11.分子和原子的主要区别是( )
| A. | 分子是构成物质的微粒,原子不是构成物质的微粒 | |
| B. | 分子由原子构成,所以分子的质量都大于原子质量 | |
| C. | 分子在不停地运动,原子在分子中不可能运动 | |
| D. | 分子在化学反应中可分,原子在化学反应中不可再分 |
15.下列与金属有关的说法正确的是( )
| A. | 黄铜是锌铜合金,其硬度比纯铜的小,熔点比纯铜的高 | |
| B. | 将铁丝和铜丝分别插入稀硫酸中可验证铁、铜的活动性强弱 | |
| C. | 生铁和钢都是铁的合金,它们属于合成材料 | |
| D. | 铝比铁更耐腐蚀,说明铁比铝金属活动性强 |
16.下列有关地球上淡水的叙述中,正确的是( )
| A. | 人类目前比较容易利用冰川水和海洋水 | |
| B. | 地球上淡水取之不尽,用之不竭 | |
| C. | 人类能利用的淡水仅占地球淡水资源的0.3% | |
| D. | 地球的淡水资源占地球总水量的71% |

