题目内容
3.用化学方程式解释下列原理.(1)除去氮气中少量的氧气4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(2)固体氢氧化钠做气体干燥剂,写出不能干燥二氧化碳的原因CO2+2NaOH═Na2CO3+H2O.
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可.
解答 解:(1)可用红磷除去氮气中少量的氧气,红磷在氧气中燃烧生成五氧化二磷,反应的化学方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
(2)二氧化碳能与氢氧化钠反应生成碳酸钠和水,反应的化学方程式是:CO2+2NaOH═Na2CO3+H2O;
故答案为:(1)4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;(2)CO2+2NaOH═Na2CO3+H2O;
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
 浙江名校名师金卷系列答案
浙江名校名师金卷系列答案
相关题目
13.科学实验室常利用浓盐酸与高锰酸钾固体反应来制取氯气:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,根据化合物中各元素化合价的代数和为零的原则,可以确定KMnO4中Mn元素的化合价为( )
| A. | +1 | B. | +2 | C. | +5 | D. | +7 |
14.下列物质露置在空气中一定不会发生化学变化的是( )
| A. | 生石灰 | B. | 氢氧化钠 | C. | 纯铝制品 | D. | 浓硫酸 |
11.规范的操作是科学实验的基本要求,下列实验操作规范的是( )
| A. | 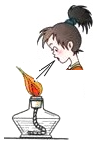 熄灭酒精灯 | B. |  倾倒液体 | ||
| C. |  将固体粉末装入试管 | D. | 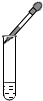 滴加液体 |
18.下列离子能在pH=1的溶液中大量共存形成无色溶液的是( )
| A. | Na+、SO42-、Cl-、Fe2+ | B. | OH-、K+、NO3-、Ba2+ | ||
| C. | Mg2+、SO42-、Al3+、NO3- | D. | Na+、CO32-、Ca2+、Cl- |
8. 烧杯中盛有 BaCl2溶液和稀盐酸100.0g,向其中滴加溶质质量分数为 10.0%的 Na2CO3溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示.下列说法正确的是( )
烧杯中盛有 BaCl2溶液和稀盐酸100.0g,向其中滴加溶质质量分数为 10.0%的 Na2CO3溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示.下列说法正确的是( )
 烧杯中盛有 BaCl2溶液和稀盐酸100.0g,向其中滴加溶质质量分数为 10.0%的 Na2CO3溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示.下列说法正确的是( )
烧杯中盛有 BaCl2溶液和稀盐酸100.0g,向其中滴加溶质质量分数为 10.0%的 Na2CO3溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示.下列说法正确的是( )| A. | ab段溶液变浑浊并伴有气泡 | |
| B. | bc段溶液质量增加 86.3g | |
| C. | c 点对应溶液的溶质质量分数为 7.5% | |
| D. | d 点溶液中溶质为 Na2CO3 |
5.以下试剂能一次鉴别氢氧化钙溶液与氢氧化钠溶液的是( )
| A. | 碳酸钠溶液 | B. | 氯化镁溶液 | C. | 稀盐酸 | D. | 酚酞溶液 |