题目内容
14.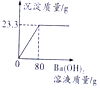 用氢氧化钡溶液测定某种氮肥中硫酸铵的质量分数(杂质溶于水,但不参加反应),实验如下:称取该氮肥20g加水完全溶解,向该溶液中不断滴入氢氧化钡溶液,生成气体及沉淀质量与加入氢氧化钡溶液的质量关系如表所示:
用氢氧化钡溶液测定某种氮肥中硫酸铵的质量分数(杂质溶于水,但不参加反应),实验如下:称取该氮肥20g加水完全溶解,向该溶液中不断滴入氢氧化钡溶液,生成气体及沉淀质量与加入氢氧化钡溶液的质量关系如表所示:| 实验次序 | 1 | 2 | 3 |
| 滴入Ba(OH)2溶液的质量/g | 20 | 40 | 60 |
| 生成气体的质量/g | 0.85 | m | 2.55 |
(1)硫酸铵中氮元素与氢元素的质量比为7:2.
(2)表格中m的值为1.70.
(3)该氮肥中硫酸铵的质量分数.
分析 根据物质的化学式可以计算组成元素的质量比;
根据表中提供的数据可以判断m的值;
根据反应的化学方程式和沉淀质量可以计算硫酸铵质量,进一步可以计算该氮肥中硫酸铵的质量分数.
解答 解:(1)硫酸铵的化学式是(NH4)2SO4,其中氮元素与氢元素的质量比为:14:4=7:2,
故填:7:2.
(2)由表中数据可知,加入20g氢氧化钡溶液时产生0.85g气体,加入60g氢氧化钡溶液时仍然产生气体,因此加入40g氢氧化钡溶液时生成1.70g沉淀,表格中m的值为1.70.
故填:1.70.
(3)设硫酸铵质量为x,
(NH4)2SO4+Ba(OH)2═BaSO4↓+2NH3↑+2H2O,
132 233
x 23.3g
$\frac{132}{x}$=$\frac{233}{23.3g}$,
x=13.2g,
该氮肥中硫酸铵的质量分数为:$\frac{13.2g}{20g}$×100%=66%,
答:该氮肥中硫酸铵的质量分数为66%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
11.规范的操作是科学实验的基本要求,下列实验操作规范的是( )
| A. | 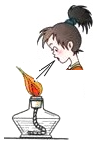 熄灭酒精灯 | B. |  倾倒液体 | ||
| C. |  将固体粉末装入试管 | D. | 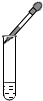 滴加液体 |
5.以下试剂能一次鉴别氢氧化钙溶液与氢氧化钠溶液的是( )
| A. | 碳酸钠溶液 | B. | 氯化镁溶液 | C. | 稀盐酸 | D. | 酚酞溶液 |
2.某氮的氧化物中,氮元素与氧元素的质量比为7:16,则该氧化物中氮元素的化合价( )
| A. | +1 | B. | +2 | C. | +3 | D. | +4 |
19.“绿色生活”是一种能源、环保的生活理念,下列行为中符合该理念的是( )
| A. | 随意丢弃旧电池 | B. | 大量燃放烟花爆竹 | ||
| C. | 将实验后的废液直接倒入水池中 | D. | 尽量选择公共交通工具出行 |
4.下列由实验事实或信息所得出的结论正确的是( )
| A. | 加压时25立方米的石油气可装入体积为0.024立方米的钢瓶中--分子在不停的运动 | |
| B. | 降低温度时某溶液中有晶体析出--该溶液降温前一定是饱和溶液 | |
| C. | 常温时某溶液能使酚酞溶液变红--该溶液一定是碱的溶液 | |
| D. | 某物质在空气中燃烧后生成二氧化碳和水--该物质中一定含有C、H元素 |
 多角度认识物质,能帮助我们更全面了解物质世界.以氧气和二氧化碳为例,回答下列问
多角度认识物质,能帮助我们更全面了解物质世界.以氧气和二氧化碳为例,回答下列问