题目内容
18.根据下表回答问题| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.5 | 37.3 | 38.4 | 39.8 |
| NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | 77.3 | |
(2)若仅采用一种操作方法,将上述烧杯中有剩余的固体全部溶解,使其变为不饱和溶液.对此有下列四种说法,其中正确的是BCD(选填字母).
A.采用的是升高温度的方法 B.溶质的质量一定增加
C.采用的是增加溶剂的方法 D.溶液的质量一定增加.
分析 (1)根据表格提供的数据,60℃时,NaCl和NH4Cl的溶解度分别是37.3g、55.2g,进行分析解答.
(2)根据表格提供的数据,氯化钠的溶解度受温度影响变化不大,氯化铵的溶解度受温度影响变化较大,进行分析解答.
解答 解:(1)根据表格提供的数据,60℃时,NaCl和NH4Cl的溶解度分别是37.3g、55.2g,则在60℃时,50g水中最多溶解氯化钠18.65g,形成的是饱和溶液;最多溶解氯化铵的质量为27.6g,故形成的是不饱和溶液.
(2)表格提供的数据,氯化钠的溶解度受温度影响变化不大,要想使氯化钠继续溶解,需要采用增加溶剂水的方法,有剩余的固体全部溶解,故溶质的质量一定增加、溶液质量一定增加.
故答案为:(1)氯化钠;(2)BCD.
点评 本题难度不大,明确氯化钠的溶解度受温度影响变化不大、饱和溶液转化为不饱和溶液的方法等是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程度,做出如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.
(1)首先对固体的成分进行确定.取少量固体于试管中,加水充分溶解,先加入足量的BaCl2 溶液,产生白色沉淀,静置后取上层清液,再加入CuSO4 溶液,产生蓝色絮状沉淀.根据实验现象,可确定该固体是氢氧化钠和碳酸钠;
(2)称取10.6g 该固体样品于锥形瓶中,加入一定质量分数的稀盐酸,直至过量,得到数据如表:计算该样品中Na2CO3的质量分数.
(1)首先对固体的成分进行确定.取少量固体于试管中,加水充分溶解,先加入足量的BaCl2 溶液,产生白色沉淀,静置后取上层清液,再加入CuSO4 溶液,产生蓝色絮状沉淀.根据实验现象,可确定该固体是氢氧化钠和碳酸钠;
(2)称取10.6g 该固体样品于锥形瓶中,加入一定质量分数的稀盐酸,直至过量,得到数据如表:计算该样品中Na2CO3的质量分数.
| 样品质量 | 反应前总质量 | 反应后总质量 |
| 10.6克 | 148.5克 | 146.3克 |
13.下列归纳方法运用正确的是( )
| A. | 铁与硫酸铜溶液、铜与硝酸银溶液、氢气和氧化铜之间都能发生置换反应,因此,置换反应不一定要在溶液中进行 | |
| B. | NaOH与CO2,SO2,SiO2都能发生反应,所以碱能与所有非金属氧化物反应 | |
| C. | 茶杯对桌面有压力,茶水对杯底有压力,大气对茶水有压力,这说明位于上面的物体对其下面的物体总存在压力 | |
| D. | 兔、狼、猩猩等哺乳动物体温恒定,由此可知体温恒定的动物属哺乳动物 |
3.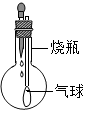 探究小组利用如图装置进行四组实验,胶头滴管盛装的是液体,烧瓶中盛装的是气体、固体或液体,当胶头滴管滴几滴液体后,能观察到气球变大的实验组合是( )
探究小组利用如图装置进行四组实验,胶头滴管盛装的是液体,烧瓶中盛装的是气体、固体或液体,当胶头滴管滴几滴液体后,能观察到气球变大的实验组合是( )
 探究小组利用如图装置进行四组实验,胶头滴管盛装的是液体,烧瓶中盛装的是气体、固体或液体,当胶头滴管滴几滴液体后,能观察到气球变大的实验组合是( )
探究小组利用如图装置进行四组实验,胶头滴管盛装的是液体,烧瓶中盛装的是气体、固体或液体,当胶头滴管滴几滴液体后,能观察到气球变大的实验组合是( )| 组合 | A | B | C | D |
| 滴管中 | Ca(OH)2 | HCl | NaOH | H2SO4(浓) |
| 烧瓶中 | HCl(气) | Zn(固) | 酚酞试液 | H2O(液) |
| A. | A | B. | B | C. | C | D. | D |
10.臭氧(O3)、二氧化氯(ClO2)、双氧水(H2O2)等物质都是生产、生活中常用的消毒剂,这三种物质都含有( )
| A. | 氧分子 | B. | 氧离子 | C. | 氧气 | D. | 氧元素 |
8.根据如图中几种物质的溶解度曲线图,得到的结论正确的是(??)
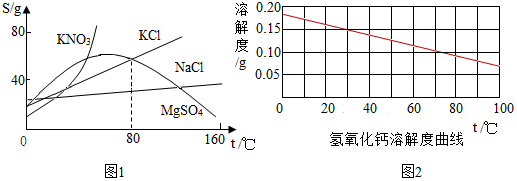

| A. | 硝酸钾中混有少量氯化钠,采用蒸发结晶进行提纯 | |
| B. | 氢氧化钙饱和溶液降低温度后有晶体析出 | |
| C. | 80℃时,氯化钾与硫酸镁的溶解度相等 | |
| D. | 所有物质的溶解度均随温度的升高而增大 |
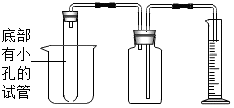 有w g颗粒状的锌铜合金.某学生利用如图所示的装置,通过测定合金与酸反应产生氢气的体积来测定合金中锌、铜的质量分数.试回答下列问题(在空格处填写相应的字母标号):
有w g颗粒状的锌铜合金.某学生利用如图所示的装置,通过测定合金与酸反应产生氢气的体积来测定合金中锌、铜的质量分数.试回答下列问题(在空格处填写相应的字母标号):