题目内容
8.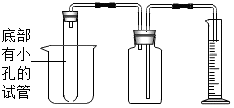 有w g颗粒状的锌铜合金.某学生利用如图所示的装置,通过测定合金与酸反应产生氢气的体积来测定合金中锌、铜的质量分数.试回答下列问题(在空格处填写相应的字母标号):
有w g颗粒状的锌铜合金.某学生利用如图所示的装置,通过测定合金与酸反应产生氢气的体积来测定合金中锌、铜的质量分数.试回答下列问题(在空格处填写相应的字母标号):(1)实验时应在烧杯、试管和广口瓶中分别加入稀硫酸、锌铜合金和蒸馏水;
(2)实验过程中的部分操作如下:a.读出量筒 内液体的体积;b.依次向烧杯与广口瓶中加入试剂;c.取出试管;d向试管中加入
试剂,置于烧杯中;正确的操作顺序是cbda;
(3)若合金与酸充分反应后,量筒中接收到的液体的体积为V L,为求出合金中锌、铜的质量分数,还缺少的一个数据是D.
A.反应前烧杯中试剂的体积 B.反应前烧杯中试剂的质量分数
C.实验前广口瓶中试剂的体积 D.实验条件下氢气的密度.
分析 根据通过测定合金与酸反应产生氢气的体积来测定合金锌、铜的质量分数,合金中是锌与稀硫酸反应产生氢气,要根据氢气求锌的质量,还需知道氢气的密度进行分析.
解答 解:(1)进行实验时,为防止生成的氢气散逸造成结果不准确,首先取出试管,向烧杯和广口瓶中加入药品,然后再向试管中加入试剂,置于烧杯中,使反应进行,反应完毕,读出读数即可,所以正确的操作顺序是:cbda;
(2)根据方程式进行的计算是物质质量间的计算,所以知道了氢气的体积,要求氢气的质量,还需要知道氢气的密度,故选:D.
故答案为:(1)cbda;
(2)D.
点评 本题考查了金属性质的应用,要测定其中某成分的含量,可以使其发生化学反应,而另一种金属不反应.根据生成物质的质量来进行起算.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
16.神舟八号,是中国“神舟”系列飞船的第八个,是一个无人目标飞行器,神八采用“长征二号”F/G火箭来发射,神舟八号发射升空后,与天宫一号对接,成为一座小型空间站.在航天飞船的失重环境中,下列实验操作最难完成的是( )
| A. | 结晶 | B. | 蒸发 | C. | 溶解 | D. | 过滤 |
13.下列条件中的氢氧化钙溶液,溶质质量分数最大的是( )
| A. | 30℃的饱和溶液 | B. | 30℃的不饱和溶液 | C. | 90℃的不饱和溶液 | D. | 90℃的饱和溶液 |
20.在一个密闭的容器中,有A、B、C、D四种物质,在一定条件下充分反应后,测得反应前后各物质的质量如下:
(1)X的值为17 g;
(2)该化学反应的反应类型是分解反应.
| 物质 | A | B | C | D |
| 反应前质量/g | 30 | 2 | 5 | 9 |
| 反应后质量/g | 5 | 15 | X | 9 |
(2)该化学反应的反应类型是分解反应.
17.下列实验操作中,不是从实验安全角度考虑的是( )
| A. | 加热试管里的液体是,先使试管底部均匀受热 | |
| B. | 托盘天平称量物品前,游码要先归零,再调节天平平衡 | |
| C. | 做铁丝在氧气中燃烧实验时,集气瓶底预先留少量的水 | |
| D. | 闭合开关前,将滑片移到滑动变阻器的阻值最大处 |
18.根据下表回答问题
(1)60℃时,向两个分别盛有25g NaCl和NH4Cl的烧杯中,各加入50g的水,充分溶解后,能成为饱和溶液的是氯化钠溶液.
(2)若仅采用一种操作方法,将上述烧杯中有剩余的固体全部溶解,使其变为不饱和溶液.对此有下列四种说法,其中正确的是BCD(选填字母).
A.采用的是升高温度的方法 B.溶质的质量一定增加
C.采用的是增加溶剂的方法 D.溶液的质量一定增加.
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.5 | 37.3 | 38.4 | 39.8 |
| NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | 77.3 | |
(2)若仅采用一种操作方法,将上述烧杯中有剩余的固体全部溶解,使其变为不饱和溶液.对此有下列四种说法,其中正确的是BCD(选填字母).
A.采用的是升高温度的方法 B.溶质的质量一定增加
C.采用的是增加溶剂的方法 D.溶液的质量一定增加.
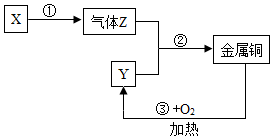 在常温下,X是一种能灭火的气态氧化物,Y是一种黑色固态氧化物,它们可以发生如图所示的转化关系:
在常温下,X是一种能灭火的气态氧化物,Y是一种黑色固态氧化物,它们可以发生如图所示的转化关系: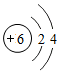 ,呈负价的离子结构
,呈负价的离子结构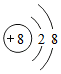 .
.