题目内容
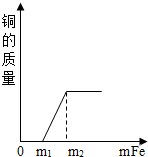
9. 有一种石灰石样品的主要成分是CaCO3.课外小组同学将100g稀盐酸分5次加入到35g石灰石样品中(已知:杂质不与盐酸反应也不溶于水),得到如下部分数据和图象.请仔细观察下列表格和图象计算:
有一种石灰石样品的主要成分是CaCO3.课外小组同学将100g稀盐酸分5次加入到35g石灰石样品中(已知:杂质不与盐酸反应也不溶于水),得到如下部分数据和图象.请仔细观察下列表格和图象计算:| 次数 | 第1次 | 第2次 | 第3次 |
| 加入盐酸的质量/g | 20 | 20 | 20 |
| 剩余固体的质量/g | 30 | a | 20 |
(2)第2次加入盐酸后,a为25g.
(3)生成二氧化碳的质量为8.8g.
(4)石灰石样品中CaCO3质量分数为多少?(结果精确到0.1%)
分析 根据反应的图象可知,在加入80g稀盐酸即第4次加入后,恰好反应完全,此后再加稀盐酸也不再会反应放出二氧化碳了,因此,前四次实验固体都得到充分反应;
根据第1次反应的数据可推知每加入20g稀盐酸,充分反应后,剩余固体减少的质量,据此规律可推断a值;
4次反应固体物质减少的质量即为样品中碳酸钙的质量,据此计算样品中碳酸钙质量分数.
解答 解:(1)碳酸钙与盐酸反应会生成二氧化碳气体,故反应中有气泡冒出;
(2)每加入20g稀盐酸固体质量将会减少35g-30g=5g,所以,第2次加入20g稀盐酸后,所剩余固体的质量=30g-5g=25g;
故答案为:25g;
(3)第4次加入稀盐酸后,固体物质总共减少的质量=5g×4=20g,设生成二氧化碳的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
20g x
$\frac{100}{44}=\frac{20g}{x}$
x=8.8g
故答案为8.8g;
(4)石灰石样品中CaCO3质量分数为:$\frac{20g}{35g}×100%$≈57.1%
答:石灰石样品中CaCO3质量分数为57.1%.
点评 根据实验记录数据,推断每加20g稀盐酸可以反应5g碳酸钙,加100g稀盐酸则需要消耗25g碳酸钙.

练习册系列答案
相关题目
20. 实验室有一瓶标签残缺的药品(如图),这瓶药品可能是( )
实验室有一瓶标签残缺的药品(如图),这瓶药品可能是( )
 实验室有一瓶标签残缺的药品(如图),这瓶药品可能是( )
实验室有一瓶标签残缺的药品(如图),这瓶药品可能是( )| A. | 氯化钾 | B. | 硝酸钾 | C. | 氢氧化钾 | D. | 硫酸钾 |
17.下列符号,只具有微观意义而不具有宏观意义的是( )
| A. | O | B. | Fe | C. | 2H2 | D. | CO2 |
2.屠嗷嗷因“发现青蒿素对疟疾寄生虫有出色疗效”而荣获诺贝尔奖.青蒿素(化学式为C15H22O5)是我国首创的新型抗疟疾药,下列关于青蒿素的叙述正确的是( )
| A. | 青蒿素中含有15个碳原子、22个氢原子、5个氧原子 | |
| B. | 青蒿素由碳、氢、氧三种元素组成 | |
| C. | 青蒿素中,C、H、O各元素质量比是15:22:5 | |
| D. | 青蒿素分子的相对分子质量是42 |