题目内容
5.如图是甲、乙两种固体物质的溶解度曲线.下列说法中不正确的是( )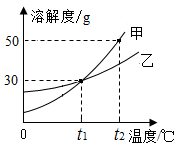
| A. | t1℃时,甲和乙的溶解度相同 | |
| B. | t2℃时,将75 g甲的饱和溶液与100 g水混合可得到溶质质量分数为20%的甲溶液 | |
| C. | t2℃时,各100 g甲、乙饱和溶液降温至t1℃,甲析出固体的质量大于乙析出固体的质量 | |
| D. | 升高温度可以将甲的饱和溶液变为不饱和溶液 |
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:A、通过分析溶解度曲线可知,t1℃时,甲和乙物质的溶解度相同,故A正确;
B、t2℃时,甲物质的溶解度是50g,所以将75g甲的饱和溶液与100g水混合可得到溶质质量分数为$\frac{50g}{150g}$×100%=33.3%的甲溶液,故B错误;
C、t2℃时,甲物质的溶解度大于乙物质的溶解度,t1℃时,甲、乙物质的溶解度相等,所以各100g甲、乙饱和溶液降温至t1℃,甲析出固体的质量大于乙析出固体的质量,故C正确;
D、甲物质的溶解度随温度的升高而增大,所以升高温度可以将甲的饱和溶液变为不饱和溶液,故D正确.
故选:B.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案
相关题目
8.有一在空气中暴露过的KOH固体,经分析知其内含:H2O 7.62%,K2CO3 2.38%,KOH 90%.若将此样品w g加入到98g20%的稀硫酸中,过量的酸再用20g10%的KOH溶液中和,恰好完全反应.蒸干中和后的溶液可得固体的质量为( )
| A. | 30.8 g | B. | 34.8 g | ||
| C. | 30.8 g~34.8 g之间 | D. | 无法计算 |
16.下列实验设计合理的是( )
| A. | 欲除去CaO中混有的CaCO3,可加入过量的稀HCl | |
| B. | 现有NaOH、稀H2SO4、NaCl、FeCl3四种溶液,不用其他试剂就可以鉴别出来 | |
| C. | 欲除去NaNO3溶液中混有的Cu( NO3)2,可先加入过量的NaOH溶液,后过滤 | |
| D. | 欲除去H2中的少量水蒸气和HCl气体,可先通入足量的浓H2SO4,后通入NaOH溶液 |
20.下列关于燃烧现象的描述,正确的是( )
| A. | 红磷在空气中燃烧产生大量的白雾 | |
| B. | 硫在空气中燃烧发出蓝紫色火焰 | |
| C. | 镁条在氧气中燃烧发出耀眼的白光,生成氧化镁 | |
| D. | 铁丝在氧气中剧烈燃烧,火星四射 |
14.19世纪末,英国物理学家瑞利在研究中发现,从空气中分离得到的氮气的密度与从含氮物质中制得的氮气的密度有0.0064千克/米3的差异.他没放过这一微小的差异,又与化学家拉姆塞合作,经过几十年的努力,终于在1894年发现了空气中的氩气.下列认识中错误的是( )
| A. | 氩气是一种化学性质极不活泼的气体 | |
| B. | 瑞利从空气中分离出的氮气是纯净物 | |
| C. | 科学研究是非常严谨的,不能放过微小的差异 | |
| D. | 从含氮物质中可以制得纯净的氮气 |
15.取一定量的氧化铁和氧化亚铁的混合物,加入200g 9.8%的稀硫酸,恰好完全反应生成盐和水.则原固体混合物中氧元素的质量是( )
| A. | 9.8 g | B. | 3.6 g | C. | 3.2 g | D. | 19.6 g |
 如图是溴元素的相关信息,请回答下列问题.
如图是溴元素的相关信息,请回答下列问题.