题目内容
15.取一定量的氧化铁和氧化亚铁的混合物,加入200g 9.8%的稀硫酸,恰好完全反应生成盐和水.则原固体混合物中氧元素的质量是( )| A. | 9.8 g | B. | 3.6 g | C. | 3.2 g | D. | 19.6 g |
分析 根据氧化铁和氧化亚铁与硫酸反应,分别生成硫酸铁和水、硫酸亚铁和水,由质量守恒定律,生成的水中的氧元素即为原固体混合物中氧元素的质量,进行分析判断.
解答 解:氧化铁和氧化亚铁与硫酸反应,分别生成硫酸铁和水、硫酸亚铁和水,由质量守恒定律,生成的水中的氧元素即为原固体混合物中氧元素的质量,则生成水的质量为200g×9.8%×$\frac{1×2}{98}$×$\frac{16}{1×2}$×100%=3.2g.
故选:C.
点评 本题有一定难度,掌握质量守恒定律、明确生成的水中的氧元素即为原固体混合物中氧元素的质量是正确解答本题的关键.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
5.如图是甲、乙两种固体物质的溶解度曲线.下列说法中不正确的是( )
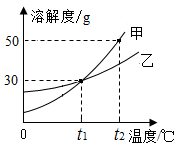

| A. | t1℃时,甲和乙的溶解度相同 | |
| B. | t2℃时,将75 g甲的饱和溶液与100 g水混合可得到溶质质量分数为20%的甲溶液 | |
| C. | t2℃时,各100 g甲、乙饱和溶液降温至t1℃,甲析出固体的质量大于乙析出固体的质量 | |
| D. | 升高温度可以将甲的饱和溶液变为不饱和溶液 |
3.现有A、B、C、D四种物质,A和B在一定条件下反应生成单质C和D,其微观模型如表所示,则下列叙述错误的是( )
| 物质 | A | B | C | D |  |
| 微观示意图 |  | 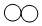 |  |  |
| A. | 该反应属于置换反应 | |
| B. | A、B、C、D的化学计量数之比为2:1:2:2 | |
| C. | 反应前后有元素的化合价发生改变 | |
| D. | 若有64 g B参加反应,则生成C的质量为64 g |
20.温室效应带来了海平面升高,病虫害加剧、土地沙化等这主要是大气中CO2含量的增加而引起的.如何防止温室效应的加剧,科子家提出多种方法,其中有人提出将CO2通过高压管道,通入深海海底储存,以减 少CO2的排放,但也有一些人提出反对意见.下列反对意见中,你认为不能成为反对理由的是( )
| A. | 将CO2通入深海海底要消耗大量能源,消耗能源也会加剧CO2的排放 | |
| B. | 海水呈弱碱性,大量CO2溶于海水生成碳酸,会使海水的酸性增大 | |
| C. | CO2是光合作用的原料,储存在海底,会使很多陆上植物的光合作用停止 | |
| D. | 当发生海底地震时,深海海底储存的CO2会被重新释放到大气中 |
7.如表是NaCl与NH4Cl在不同温度时的溶解度数据,下列说法正确的是( )
| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| NaCl | 35.7g | 36.0g | 36.6g | 37.3g | 38.4g |
| NH4Cl | 29.4g | 37.2g | 45.8g | 55.2g | 65.6g |
| A. | NaCl的溶解度比NH4Cl小 | |
| B. | 控制温度在0~20℃之间时,两种物质可配出质量分数相同的饱和溶液 | |
| C. | NaCl中含有少量NH4Cl时,可通过冷却热饱和溶液的方法来提纯NaCl | |
| D. | 80℃时将两种物质各5 g分别加入到10 g水中,固体均能全部溶解 |
4.下列古代生产工艺中主要体现的物理变化的是( )
| A. | 粮食酿酒 | B. | 纺纱织布 | C. | 烧制瓷器 | D. | 冶炼生铁 |