题目内容
1.硫酸铜的构成微粒有Cu2+和SO42-;在医疗上可以小苏打治疗胃酸(HCl)过多症,其原理是NaHCO3+HCl=NaCl+H2O+CO2↑(用化学方程式表示).分析 硫酸铜是由铜离子和硫酸根离子构成的;
小苏打是碳酸氢钠的俗称,能和胃酸中的稀盐酸反应生成氯化钠、水和二氧化碳.
解答 解:硫酸铜的构成微粒有Cu2+和SO42-;
在医疗上可以小苏打治疗胃酸(HCl)过多症,其原理是碳酸氢钠能和胃酸中的稀盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为:NaHCO3+HCl=NaCl+H2O+CO2↑.
故填:SO42-;NaHCO3+HCl=NaCl+H2O+CO2↑.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案
相关题目
12.小金利用图示装置进行甲、乙对比实验,探究温度对CO和Fe2O3反应的影响(固定装置略).
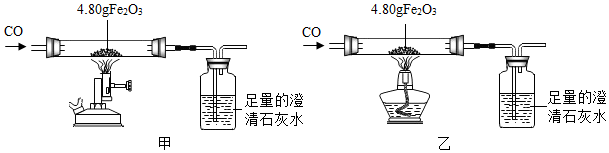
(1)从实验安全角度考虑,图示装置还应采取的改进措施是导管后放点燃的酒精灯或在导管后扎气球.
(2)完全反应后,两组的生成物均为黑色粉未(纯净物),分别用两组生成物进行以下实验:
①甲组的黑色粉末与稀盐酸反应的化学方程式是Fe+2HCl═FeCl2+H2↑.
②小金查阅资料后发现Fe3O4在常温下不与稀盐酸、CuSO4溶液反应,故猜想乙组的生成物为Fe3O4.他又发现m2恰好为4.64g,这可成为支持上述猜想的新证据.
(3)甲、乙两组实验说明温度对CO和Fe2O3反应影响,且均体现出CO的还原性(填写化学性质).

(1)从实验安全角度考虑,图示装置还应采取的改进措施是导管后放点燃的酒精灯或在导管后扎气球.
(2)完全反应后,两组的生成物均为黑色粉未(纯净物),分别用两组生成物进行以下实验:
| 步骤 | 操作 | 甲组现象 | 乙组现象 |
| 1 | 称量黑色粉末质量/g | m1 | m2 |
| 2 | 取黑色粉末,用磁铁吸引 | 能被吸引 | 能被吸引 |
| 3 | 取黑色粉未,加入稀盐酸 | 全部溶解,有大量气泡 | 无明显现象 |
| 4 | 取黑色粉末,加入足量CuSO4溶液 | 有红色物质生成 | 无明显现象 |
②小金查阅资料后发现Fe3O4在常温下不与稀盐酸、CuSO4溶液反应,故猜想乙组的生成物为Fe3O4.他又发现m2恰好为4.64g,这可成为支持上述猜想的新证据.
(3)甲、乙两组实验说明温度对CO和Fe2O3反应影响,且均体现出CO的还原性(填写化学性质).
6.安顺生产茶叶,茶叶中含锌、硒、茶氨酸(化学式为C7H14O3N2)等多种成分,茶树适宜在pH为5-6的土壤中生长.下列说法不正确的是( )
| A. | 茶氨酸由碳、氢、氧、氮四种元素组成 | |
| B. | 茶树不宜在碱性土壤中生长 | |
| C. | 一个茶氨酸分子中含有3个氧原子 | |
| D. | 茶叶中的锌、硒指单质,茶氨酸属于有机物 |
13.如图为某反应的微观示意图,其中代表不同元素的原子.下列说法正确的是( )


| A. | 有五种分子参加反应 | |
| B. | 有两种分子参加反应且个数比为3:1 | |
| C. | 各元素的化合价在反应前后未改变 | |
| D. | 此化学反应属于置换反应 |
11.把下列物质分别放入水中,充分搅拌,可以得到溶液的是( )
| A. | 碘 | B. | 面粉 | C. | 蔗搪 | D. | 花生油 |