题目内容
9.如图是初中化学中常见物质间的转化关系,其中只有甲为单质,其他都是化合物;A是植物进行光合作用的一种重要原料,C可用于中和酸性土壤.反应②属于中和反应,图中“-”表示两端的物质能发生化学反应;“→”表示物质间存在转化关系,其余反应条件、部分反应物和生成物均已略去.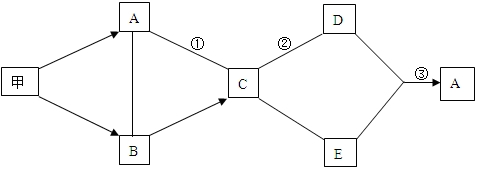
试推断:
(1)A物质的化学式CO2;B到C的化学反应类型属于化合反应(填写化合反应、分解反应、置换反应或者复分解反应);复分解反应发生后,生成物肯定不会是单质(填“单质”或“化合物”).
(2)写出反应③的化学方程式:Na2CO3+2HCl=2NaCl+H2O+CO2↑.
分析 本题属于推断题,根据题目给出的流程图和信息:其中只有甲为单质,其他都是化合物;A是植物进行光合作用的一种重要原料,因此A是二氧化碳;C可用于中和酸性土壤,氧气和氢气在点燃的条件下生成水,氧化钙和水生成氢氧化钙,因此甲是氧气,B是水,C是氢氧化钙;氢氧化钙和碳酸钠反应生成碳酸钙白色沉淀和氢氧化钠,因此E是碳酸钠;反应②属于中和反应,因此D是稀盐酸(或稀硫酸),碳酸钠和盐酸反应生成氯化钠和水和二氧化碳.
解答 解:(1)根据题目给出的流程图和信息:其中只有甲为单质,其他都是化合物;A是植物进行光合作用的一种重要原料,因此A是二氧化碳;C可用于中和酸性土壤,氧气和氢气在点燃的条件下生成水,氧化钙和水生成氢氧化钙,属于化合反应;复分解反应发生后,生成物肯定不会是单质;故答案为:CO2,化合反应,单质;
(2)碳酸钠和盐酸反应生成氯化钠和水和二氧化碳,配平即可,故答案为:Na2CO3+2HCl=2NaCl+H2O+CO2↑;
点评 本考点属于物质的推断题,是通过对实验方法和过程的探究,在比较鉴别的基础上,得出了正确的实验结论.本考点是中考的重要内容之一,一般有两种类型:一是图框式推断题;二是文字描述型推断题;本题属于第一种类型.不论哪一种类型,都是通过实验现象,从而得出物质的组成.此考点主要出现在填空题和实验题中.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
16.密闭容器中盛有CH4和O2的混合气体,点燃使其充分反应,CH4全部转化为CO、CO2和H2O,待容器恢复至室温,测得容器内混合气体中碳元素的质量分数为36%.则反应前CH4和O2的质量比为( )
| A. | 4:13 | B. | 3:10 | C. | 2:7 | D. | 1:4 |
20.下列物质的用途错误的是( )
| A. |  聚乙烯塑料做电线外皮 | B. |  酱油中添加铁元素 | ||
| C. |  石灰石做建筑材料 | D. |  木炭吸附一些食品里的色素 |
17.下面是兴趣小组同学对暴露在空气的氢氧化钠固体的探究.请回答下列问题:
[提出问题 1]:
该氢氧化钠固体有没有变质呢?
[进行实验 1]:甲同学取少量固体于试管中用足量的水溶解,后加入过量的 BaCl2 溶液,观察到产生白色沉淀,证明氢氧化钠固体已经含有 Na2CO3.
[提出问题 2]:
如何除去氢氧化钠固体中的杂质,得到纯净的氢氧化钠呢?
[进行实验 2]:乙同学对该氢氧化钠固体进行提纯,按如下操作流程进行实验.
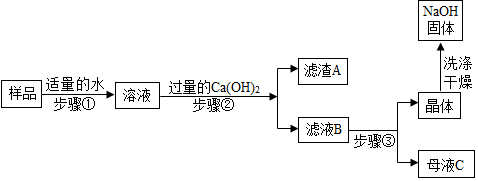
[实验分析]:
(1)步骤②反应的化学方程式是Na2CO3+Ca(OH)2═CaCO3↓+2NaOH,步骤②的操作有搅拌 和过滤,搅拌的作用是使碳酸钠完全反应.
(2)证明步骤②中已达到 Ca(OH)2溶液过量的目的,下列方案中可行的是ac.
a.取少量滤液 B,向其中通二氧化碳气体,溶液变浑浊
b.取少量溶液 B,向其中再加少量石灰水,无白色浑浊
c.取少量溶液 B,向其中再加少量浓碳酸钠溶液,有白色浑浊
(3)为获得纯净的氢氧化钠步骤③所包含的具体操作是蒸发浓缩、B、过滤. A.蒸发结晶B.降温结晶
(4)丙同学认为乙同学流程中的 Ca(OH)2 溶液可以用稍过量的 Ba(OH)2 溶液代替,代替后的主要优点是A.
A.氢氧化钙微溶于水,氢氧化钡易溶于水,用氢氧化钡溶液可以减少溶液中水的量,以提高蒸发浓缩的效率,并节约能源.
B.只有氢氧化钡才能除去杂质[实验拓展]:如何测定久置的烧碱样品中氢氧化钠的质量分数呢?
从一瓶久置的烧碱中称取了 20g,干燥后剩余固体固体质量为 19g,完全溶于蒸馏水 中配成 100g 样品溶液,现取一定溶质的质量分数的氯化钡溶液与样品溶液混合,充分反 应后得到如表所示的数据.
(5)表中第2、4次恰好完全反应.
(6)请计算样品中氢氧化钠的质量分数?(请保留具体解题过程)
[提出问题 1]:
该氢氧化钠固体有没有变质呢?
[进行实验 1]:甲同学取少量固体于试管中用足量的水溶解,后加入过量的 BaCl2 溶液,观察到产生白色沉淀,证明氢氧化钠固体已经含有 Na2CO3.
[提出问题 2]:
如何除去氢氧化钠固体中的杂质,得到纯净的氢氧化钠呢?
[进行实验 2]:乙同学对该氢氧化钠固体进行提纯,按如下操作流程进行实验.

[实验分析]:
(1)步骤②反应的化学方程式是Na2CO3+Ca(OH)2═CaCO3↓+2NaOH,步骤②的操作有搅拌 和过滤,搅拌的作用是使碳酸钠完全反应.
(2)证明步骤②中已达到 Ca(OH)2溶液过量的目的,下列方案中可行的是ac.
a.取少量滤液 B,向其中通二氧化碳气体,溶液变浑浊
b.取少量溶液 B,向其中再加少量石灰水,无白色浑浊
c.取少量溶液 B,向其中再加少量浓碳酸钠溶液,有白色浑浊
(3)为获得纯净的氢氧化钠步骤③所包含的具体操作是蒸发浓缩、B、过滤. A.蒸发结晶B.降温结晶
(4)丙同学认为乙同学流程中的 Ca(OH)2 溶液可以用稍过量的 Ba(OH)2 溶液代替,代替后的主要优点是A.
A.氢氧化钙微溶于水,氢氧化钡易溶于水,用氢氧化钡溶液可以减少溶液中水的量,以提高蒸发浓缩的效率,并节约能源.
B.只有氢氧化钡才能除去杂质[实验拓展]:如何测定久置的烧碱样品中氢氧化钠的质量分数呢?
从一瓶久置的烧碱中称取了 20g,干燥后剩余固体固体质量为 19g,完全溶于蒸馏水 中配成 100g 样品溶液,现取一定溶质的质量分数的氯化钡溶液与样品溶液混合,充分反 应后得到如表所示的数据.
| 项目和次数 | 第 1 次 | 第 2 次 | 第 3 次 | 第 4 次 |
| 样品溶液质量(g) | 10 | 20 | 30 | 40 |
| 氯化钡溶液质量(g) | 10 | 15 | 15 | 30 |
| 产生沉淀的质量(g) | 1.97 | 3.94 | 3.94 | X |
(6)请计算样品中氢氧化钠的质量分数?(请保留具体解题过程)
14.如图是对实验绘制的相关变化的图形,其中实验结果与图形对应准确的是( )
| A. | 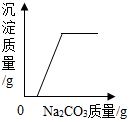 向氯化氢和氯化钙的混合溶液中加入碳酸钠溶液,生成沉淀质量的变化 | |
| B. | 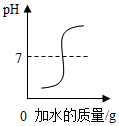 向硫酸中加水,溶液pH的变化 | |
| C. | 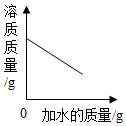 向饱和食盐水中不断加水,溶液中溶质的质量变化 | |
| D. | 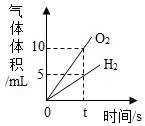 电解水生成气体的体积 |