题目内容
17.除去下列物质中的杂质,所选用的方法正确的是( )| 物质(括号内为杂质) | 搡作方法 | |
| A | CO2(HCl) | 先通过过量氧化钠溶液,再通过浓硫酸 |
| B | NaCl溶液(Na2CO3) | 加稀硫酸恰好不再产生气泡为止 |
| C | CuSO4溶液(H2SO4) | 加过量氧化铜粉末充分反应后过滤 |
| D | 铁粉(铜粉) | 加过量FeSO4溶液充分反应后过滤、干燥 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、CO2和HCl气体均能与NaOH溶液反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
B、Na2CO3能与稀硫酸反应生成硫酸钠、水和二氧化碳,能除去杂质但引入了新的杂质硫酸钠,不符合除杂原则,故选项所采取的方法错误.
C、H2SO4能与过量氧化铜粉末反应生成硫酸铜和水,充分反应后过滤,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
D、铜粉不能与FeSO4溶液反应,不能除去杂质,不符合除杂原则,故选项所采取的方法错误.
故选:C.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
7.铜与浓硫酸发生的反应为:Cu+2H2SO4(浓)═CuSO4+SO2↑+2H20.有关CuSO4制备途径及性质如图所示,下列说法错误的是( )


| A. | 反应①②中均有一种元素的化合价发生变化 | |
| B. | 反应③和④中的铜元素质量未发生改变 | |
| C. | 途径②比途径①更好地体现了绿色化学思想 | |
| D. | 反应④说明某些碱受热分解生成金属氧化物 |
5.下列应用的原理用化学方程式表示正确的是( )
| A. | 用锌与稀盐酸制氢气:2Zn+2HCl═2ZnCl+H2↑ | |
| B. | 用红磷燃烧测定空气中氧气含量:S+O2 $\frac{\underline{\;点燃\;}}{\;}$SO2 | |
| C. | 用一氧化碳作燃料:CO+O2 $\frac{\underline{\;点燃\;}}{\;}$CO2 | |
| D. | 高温煅烧石灰石制取二氧化碳:CaCO3 $\frac{\underline{\;高温\;}}{\;}$ CaO+CO2↑ |
6.括号内是区别下列各组常见物质的方法,其中正确的是( )
| A. | 碳粉和二氧化锰(加双氧水) | B. | 二氧化碳和氮气(用燃着的木条) | ||
| C. | 蒸馏水与食盐水(过滤) | D. | 硬水和澄清石灰水(加肥皂水) |
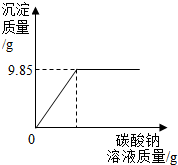 某化工厂技术员小李分析氯化钡和氯化钠组成的产品中氯化钠的质量分数,取16.25g固体样品全部溶于143.6g水中,向所得溶液中滴加溶质质量分数为10.6%的碳酸钠溶液,记录了如图表示的曲线关系.
某化工厂技术员小李分析氯化钡和氯化钠组成的产品中氯化钠的质量分数,取16.25g固体样品全部溶于143.6g水中,向所得溶液中滴加溶质质量分数为10.6%的碳酸钠溶液,记录了如图表示的曲线关系.

 ,该粒子所属元素位于周期表的第三周期;
,该粒子所属元素位于周期表的第三周期;