题目内容
1.请回忆你曾观察、学习过的二组实验.第一组实验:取四朵用石蕊溶液染成紫色的干燥的纸花,分别按如图1进行实验.

| (I) | (II) | (III) | (IV) | |
| 现象 | 紫色纸花变红 | 紫色纸花不变色 | 紫色纸花不变色 | 紫色纸花变红 |
分析 | ①验(III)验证了:二氧化碳不能使紫色石蕊变红 实验(Ⅳ)验证了;二氧化碳的水溶液能使紫色石蕊变红 ②通过实验(I)、(Ⅳ),可验证酸的一条化学性质是:酸能使紫色石蕊溶液变红 ③实验(Ⅳ)结束后,将纸花用酒精灯小心加热烘烤后纸花又变紫,说明碳酸热稳定性差,受热易分解. | |||
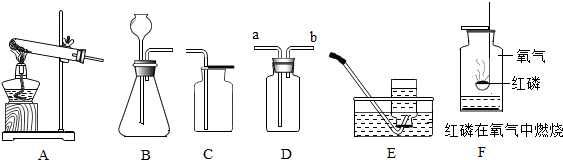
(1)某同学按图2装置对质量守恒定律进行实究,观察到反应后天平不平衡,该反应质量守恒定律符合(填“符合”或“不符合”),天平不平衡的理由是反应生成的CO2气体逸出,导致天平不平衡.
(2)由质量守恒定律可知,化学反应前后,一定不变的是①②⑤(填序号).
①原子种类 ②原子数目 ③分子种类 ④分子数目 ⑤元素种类 ⑥物质种类
(3)硝酸在工业生产中且有广泛的应用.工业上制取硝酸的关键反应为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6R
,其中R的化学式为H2O(填化学式).
分析 第一组实验:显酸性的溶液能使石蕊试液变红色,二氧化碳不能使石蕊试液变红色,二氧化碳能和水反应生成碳酸,碳酸能使石蕊试液变红色;
碳酸不稳定,受热容易分解生成水和二氧化碳.
第二组实验:(1)化学变化都遵循质量守恒定律,由于碳酸钠与盐酸反应产生的二氧化碳气体没有在所称的质量内,所以反应后因气体逸散天平不平衡;
(2)化学变化是分子分成原子然后原子重新结合成新的分子的过程,在此过程中,分子发生了改变,由分子构成的物质也发生了改变;
(3)根据化学变化前后原子的种类和个数不变,根据反应物的分子构成及参加反应的分子个数,推断生成物R的分子构成.
解答 解:第一组实验:
喷水后的紫花放入二氧化碳中,紫花变红色,是因为水和二氧化碳反应生成了碳酸,碳酸使紫色石蕊变红色.
故填:紫色纸花变红.
①实验Ⅲ中的紫花不变色,验证了二氧化碳不能使紫色石蕊变红;
实验Ⅳ验证了二氧化碳的水溶液能使紫色石蕊变红.
故填:二氧化碳不能使紫色石蕊变红;二氧化碳的水溶液能使紫色石蕊变红.
②通过实验Ⅰ、Ⅳ,可验证酸能使紫色石蕊溶液变红.
故填:酸能使紫色石蕊溶液变红.
③实验Ⅳ结束后,将纸花用酒精灯小心加热烘烤后纸花又变紫,说明碳酸的热稳定性差,受热易分解.
故填:热稳定性差,受热易分解.
第二组实验:
(1)由于装置没有密封,碳酸钠与盐酸反应产生的气体二氧化碳逸散到空气中,而使反应前后天平不平衡;如果二氧化碳气体不逸出,反应前后天平保持平衡;这一现象也从另一方面说明了反应是遵循质量守恒的;
故填:符合;反应生成的CO2气体逸出,导致天平不平衡;
(2)在化学变化过程中,原子是最小的微粒,原子的种类、个数一定不变,组成物质的元素的种类也一定不变;而分子的种类、物质的种类是一定发生改变的;分子的数目有时也会相等;
故填:①②⑤;
(3)反应前N、H、O元素的原子个数分别为4、12、10;而反应后4NO中含4个N、4个O原子,根据反应前后原子种类、个数不变,6个R分子中应含有12个H原子和6个O原子,则每个R分子由2个H原子和1个O原子构成,其化学式为H2O;
故填:H2O;
点评 实验现象是物质之间相互作用的外在反映,要学会设计实验、分析实验,善于根据实验现象总结事物之间的内在联系.

| 物质 | A | B | C | D |
| 肥皂水 | 食醋 | 牙膏 | 食盐水 | |
| pH | 10 | 3 | 9 | 7 |
(2)做馒头发酵面团时,会产生乳酸等有机酸,蒸馒头前需加进适量的纯碱或小苏打等碱性物质,它们相互作用产生了CO2气体(填化学式),使蒸出的馒头疏松多孔;若加入的碱性物质过多,可向面团或蒸锅中滴加少许含食醋(填物质名称)的酸性调味料,否则蒸出的馒头会变涩,颜色发黄.
(3)未成熟的水果大多具有涩味,这是因为水果里含有鞣酸.脱涩的方法之一是:先用少量的水将生石灰化成石灰乳,该变化的化学方程式是CaO+H2O═Ca(OH)2,然后把它用清水稀释,取上层清夜,浸泡水果5至6天即可除去涩味.
(4)人被昆虫叮咬后皮肤红肿起泡,这是由于昆虫在皮肤内注入了少量甲酸所致.把少许如表所列的生活常用品A或C(填编号)涂在被咬的皮肤上,痛痒便会消失.
(5)请你再举出一种生产、生活中常见的利用酸碱的例子用熟石灰改良酸性土壤.
| 温度/℃ | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| 溶解度/g | 122 | 130 | 140 | 160 | 190 | 220 | 250 |
(1)上述所得溶液是否饱和?(要求写出判断依据)
(2)若上述溶液不饱和,用哪些方法可使溶液转化为饱和溶液?