题目内容
9. 某实验小组设计了测定空气中氧气含量的实验,装置如图所示.该实验中,红磷需稍过量,待燃烧停止,装置冷却后,打开止水夹,观察烧杯中的水进入集气瓶,瓶内水面最终接近刻度$\frac{1}{5}$处.由此可知,氧气约占空气总体积的$\frac{1}{5}$.
某实验小组设计了测定空气中氧气含量的实验,装置如图所示.该实验中,红磷需稍过量,待燃烧停止,装置冷却后,打开止水夹,观察烧杯中的水进入集气瓶,瓶内水面最终接近刻度$\frac{1}{5}$处.由此可知,氧气约占空气总体积的$\frac{1}{5}$.(1)由本实验还可推知氮气的哪些性质?试写出其中的一条物理性质难溶于水 和化学性质不支持燃烧.
(2)若将红磷换成炭粉,该实验能否成功?否(填“能”或“否”).
(3)若进入瓶中的水的高度略大于$\frac{1}{5}$刻度,则可能的原因是什么?点燃红磷后没有迅速伸入瓶中,而是在瓶中停留时间过长.
分析 本题是测定空气中氧气的含量,我们常用燃烧红磷或白磷的方法,因为磷燃烧生成白色固体五氧化二磷,几乎不占空间,使得内外产生气压差,从而得到正确的结论.因此在选择可燃物时,必须考虑到:燃烧的条件;生成物的状态;不与空气中其他物质发生反应.保证本实验成功的关键是:①装置气密性好;②红磷要足量;③要冷却至室温再读数.
解答 解:(1)根据烧杯中的水进入集气瓶,瓶内水面最终接近刻度1处可知,氧气约占空气体积的$\frac{1}{5}$;水倒流入集气瓶中的体积只有的$\frac{1}{5}$,若氮气易溶于水,则倒流入瓶内的水几乎会充满整个集气瓶,因此氮气是难溶于水的;红磷燃烧一会熄灭了,说明氮气不燃烧不支持燃烧,其化学性质不活泼;
(2)炭粉燃烧消耗氧气,同时生成二氧化碳气体,集气瓶内压强基本不变.故不能将红磷换成炭粉;
(3)若进入瓶中的水的高度略大于$\frac{1}{5}$刻度,则可能的原因是点燃红磷后没有迅速伸入瓶中,而是在瓶中停留时间过长.
故答案为:(1)难溶于水;不支持燃烧;(2)否;(3)点燃红磷后没有迅速伸入瓶中,而是在瓶中停留时间过长.
点评 本题主要考查用红磷测定空气组成的实验原理、操作、现象、结论和注意事项,难度稍大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
19.生活在一些常见液体的pH值如下,其中酸性最强的是( )
| A. | 玉米粥6.8 | B. | 橙汁3.5 | C. | 肥皂水11 | D. | 洗发露7.6 |
20.下列物质鉴别的方法错误的是( )
| A. | 区别二氧化碳、氧气和空气--分别将燃着的木条伸入瓶中,观察现象 | |
| B. | 区别过氧化氢和蒸馏水--加入MnO2,看是否有气泡 | |
| C. | 区别硬水与软水--常用肥皂水检验,泡沫减少产生浮渣的是硬水 | |
| D. | 区别二氧化锰和氧化铜--观察颜色 |
17.下列关于碳的单质和氧化物的组成、性质和用途的说法中,错误的是( )
| A. | 璀璨夺目的天然钻石和黑乎乎的碳粉外观差异很大,但它们都是由碳元素组成的 | |
| B. | 长期未用而难开启的铁锁,可在锁孔中加入少量铅笔芯粉末作润滑剂 | |
| C. | 干冰用于人工降雨和制冷剂,是利用其化学性质 | |
| D. | 可用活性炭除去糖浆里的色素,这是利用它的物理性质--吸附性 |
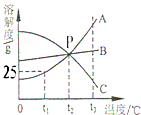 如图为A、B、C三种物质的溶解度曲线,据图回答:
如图为A、B、C三种物质的溶解度曲线,据图回答: