��Ŀ����
����Ŀ��С�մ�̼�����ƣ����ճ��������й㷺����;����ҵ����ȡС�մ��ж��ַ�����������һ���������̼���������õ�ԭ���ǣ�Na2CO3 + H2O + CO2 =2NaHCO3
���ϣ�̼���ƺ�̼�����Ƶ��ܽ�ȱ���һ��������ѹ�£������֣�
�¶�/�� | 0 | 15 | 20 | 30 | 40 | 50 | 60 |
̼�������ܽ��/g | 6.9 | 8.72 | 9.6 | 11.1 | 12.7 | 14.45 | 16.4 |
̼�����ܽ��/g | 7.1 | 13.25 | 21.8 | 39.7 | 48.8 | 47.3 | 46.4 |
ͬѧ�Ƕ���ظ�ʵ�飬����ʵ��������һ�¡���ͬѧ���������10minʱ��Һ�����ʵ���ɣ�����ͬѧ���������ʵ�鷽������ʵ�顣
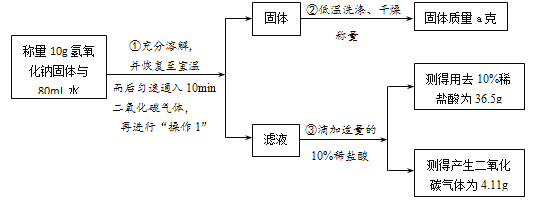
�� ʵ�鲽����У�������1����________��ʵ�鲽����У�Ϊ��֤����ϡ����������ȷ����ӦԤ�Ƚ��е�ʵ�������________��
�� ͨ�����ݷ�����ͨ��10min������̼ʱ��Һ������������________��ʵ���С���������a�ˡ���a�����ֵ��________��
���𰸡� ���� ��Һ��ӦԤ�ȵμ���ɫ��̪ Na2CO3��Na H CO3 12.6g
����������1�����˿ɽ�������Һ��ֿ���Ϊ��֤����ϡ����������ȷ��Ӧ������Һ��ӦԤ�ȵμ���ɫ��̪������Һǡ�ñ�Ϊ��ɫ��ֹͣ�μ����ᡣ
��2��ͨ�����ݷ���������ʱ�й�������˵��̼�����ƹ���Ϊag��
������36.5g10%��ϡ����ȫ����̼�����Ʒ�Ӧ���ų��Ķ�����̼������Ϊx
NaHCO3+HCl=NaCl+ H2O + CO2��
36.5 44
36.5g��10% x
![]()
x=4.4g��4.11g
ͨ��10min������̼ʱ��Һ������������Na2CO3��NaHCO3��
10g������������Ԫ�ص�����Ϊ10g��![]() =5.75g
=5.75g
������������ȫ��ת��Na2CO3��NaHCO3������NaHCO3+HCl=NaCl+ H2O + CO2����Na2CO3+2HCl=2NaCl+ H2O + CO2����֪��
����Һ�е���Ԫ��Ϊy
HCl��NaCl��Na
36.5 23
36.5g��10% y
![]()
y=2.3g
���Խ���̼�����ƾ������Ԫ�ص�����Ϊ5.75g-2.3g=3.45g��
������̼�����ƾ��������Ϊ![]() =12.6g��
=12.6g��