题目内容
11.1993年1月18日,第四十七届联合国大会作出决议,确定每年的3月22日为“世界水日(World Water Day)”.这个节日的确定是为了“向全世界发出严正警告:水不久将成为一个深刻的社会危机”,如果人类继续破坏和浪费水资源,那么人类看到的最后一滴水将是自己的眼泪.下列有关水的知识,其中不正确的是( )| A. | 水是一种最常见的溶剂,自然界中的水都不是纯净物 | |
| B. | 酸雨的形成与大气中SO2等酸性污染物增多有关 | |
| C. | 水中N、P元素的增多会引起水体的富营养化污染,引起赤潮和水华 | |
| D. | pH=0的水溶液,是中性的溶液 |
分析 A、根据水的组成的分析;
B、根据形成酸雨气体的种类为分析;
C、根据赤潮和水华形成的原因分析;
D、根据溶液的酸碱性与酸碱度的关系分析.
解答 解:A、水是一种最常见的溶剂,自然界中的水常混入可溶、不可溶性的杂质,都不是纯净物,故A正确;
B、酸雨的形成与大气中SO2等酸性污染物增多有关,故B正确;
C、水中N、P元素的增多会引起水体的富营养化污染,引起赤潮和水华,故C正确;
D、pH=0的水溶液,是酸性的溶液,故D错误.
故选D.
点评 本题考查的知识主要是与水有关的知识,属于课本中的基础知识,难度不大,根据已有的知识分析解答即可.

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案
相关题目
2.某工厂用电解饱和食盐水的方法生产氯气、烧碱、氢气等化工产品(反应的化学方 程式:2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑),这种工业称为“氯碱工业”.某研究性学习小组对该厂生产的烧碱样品进行如下探究.
Ⅰ.定性探究
【提出问题】烧碱样品中可能含有哪些杂质?
【猜想】猜想一:可能含有Na2C03,作出此猜想的依据是CO2+2NaOH=Na2CO3+H2O(用化学方程式表示).
猜想二:可能含有NaCl,作出此猜想的依据是可能有少量的氯化钠没有反应(用简洁的文字表述).
【设计实验】
【交流与讨论】小明同学提出:“上述实验中稀硝酸也可以用稀盐酸代替”.你认为他的观点不正确(填“正确”或“不正确”).
Ⅱ.定量探究
【提出问题】烧碱样品中氢氧化钠的质量分数是多少呢?
【设计实验】小婉同学设计探究方案后进行实验并测得数据如下:
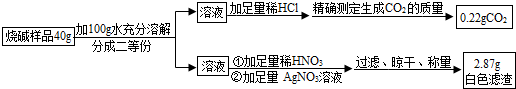
请你利用小婉同学测得的数据计算烧碱样品中氢氧化钠的质量分数(请列出计算过程).
Ⅰ.定性探究
【提出问题】烧碱样品中可能含有哪些杂质?
【猜想】猜想一:可能含有Na2C03,作出此猜想的依据是CO2+2NaOH=Na2CO3+H2O(用化学方程式表示).
猜想二:可能含有NaCl,作出此猜想的依据是可能有少量的氯化钠没有反应(用简洁的文字表述).
【设计实验】
| 实验步骤 | 实验现象 | 解释或结论 |
| ①取适量烧碱样品置于试管中,加水溶解,并用手触摸试管外壁. | 试管外壁发热 | 原因是氢氧化钠固体溶于水放热 |
| ②向①所得的溶液中逐滴加入稀硝酸至过量 | 一开始无明显现象,一段时间后产生能使澄清石灰水变浑浊的气体. | 样品中含有的杂质是碳酸钠 |
| ③向②所得的溶液中滴加几滴硝酸银溶液 | 产生白色沉淀 | 样品中还含有的杂质是氯化钠 |
Ⅱ.定量探究
【提出问题】烧碱样品中氢氧化钠的质量分数是多少呢?
【设计实验】小婉同学设计探究方案后进行实验并测得数据如下:

请你利用小婉同学测得的数据计算烧碱样品中氢氧化钠的质量分数(请列出计算过程).
16.镧(La)元素的氧化物的化学式为La2O3,La(OH)3是不溶于水的碱,而LaCl3、La(NO3)3都可溶于水.由此判断下列几组物质,不能直接反应制取LaCl3的是( )
| A. | La(OH)3和HCl | B. | La2O3和HCl | C. | La和HCl | D. | NaCl和La(OH)3 |
3.仅通过如图实验现象,下列说法不合理的是( )


| A. | 此实验能证明大气压的存在 | |
| B. | 如果要证明CO2会与NaOH反应,还需要用水来做对照 | |
| C. | CO2被NaOH溶液吸收后,瓶内气压一定减小 | |
| D. | 此实验证明CO2既会与NaOH反应,又会与水反应 |
20.通过一个月的化学学习,应该知道有多种途径可以制取氧气.如:

A.电解水 B.分离空气 C.加热高锰酸钾 D.分解过氧化氢 E.加热氯酸钾和二氧化锰的混合物
(1)请在E处写出另一种制取氧气的文字反应式氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气;
(2)若用如图1装置加热高锰酸钾制取氧气,实验结束,停止加热时要先把导管移出水面,其理由是防止水槽中水倒流,炸裂试管
不用填,此时发现水槽中的水变成了浅紫红色,你认为产生该现象的原因可能是试管口没有放一团棉花;
(3)若分解过氧化氢制取氧气,供选用的装置如图2所示.
要得到平稳的氧气流,应选用的发生装置是甲(选填“甲”或“乙”);
若用丙装置收集生成的氧气,气体应从a(选填“a”或“b”)端导入.
(4)同学们想探究双氧水的溶质质量分数对反应速率的影响.在其他条件相同的情况下进
行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
①如图3所示,取用二氧化锰的仪器是B(选填编号).
②请写出过氧化氢分解的文字反应式过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.
③实验3中,加入的二氧化锰质量为5g.
④相同条件下,实验3产生氧气的速率最快,说明在相同的条件下,双氧水的溶质质量分数越大,反应速率越快.

A.电解水 B.分离空气 C.加热高锰酸钾 D.分解过氧化氢 E.加热氯酸钾和二氧化锰的混合物
(1)请在E处写出另一种制取氧气的文字反应式氯酸钾$→_{加热}^{二氧化锰}$氯化钾+氧气;
(2)若用如图1装置加热高锰酸钾制取氧气,实验结束,停止加热时要先把导管移出水面,其理由是防止水槽中水倒流,炸裂试管
不用填,此时发现水槽中的水变成了浅紫红色,你认为产生该现象的原因可能是试管口没有放一团棉花;
(3)若分解过氧化氢制取氧气,供选用的装置如图2所示.
要得到平稳的氧气流,应选用的发生装置是甲(选填“甲”或“乙”);
若用丙装置收集生成的氧气,气体应从a(选填“a”或“b”)端导入.
(4)同学们想探究双氧水的溶质质量分数对反应速率的影响.在其他条件相同的情况下进
行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
| 实验 | 30%双氧水的质量(g) | 加入的水的体积(mL) | 二氧化锰质量(g) | 收集时间(s) |
| 1 | 10 | 40 | 5 | 200 |
| 2 | 20 | 30 | 5 | 100 |
| 3 | 30 | 20 | 5 | 67 |
②请写出过氧化氢分解的文字反应式过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.
③实验3中,加入的二氧化锰质量为5g.
④相同条件下,实验3产生氧气的速率最快,说明在相同的条件下,双氧水的溶质质量分数越大,反应速率越快.
1.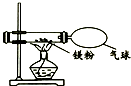 某兴趣小组为了验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组为了验证质量守恒定律,做了镁条在空气中燃烧的实验.
(1)请写出镁条与氧气反应的化学方程式2Mg+O2 $\frac{\underline{\;点燃\;}}{\;}$2MgO.
(2)小霖发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵守质量守恒定律.我不同意
(填“同意”或“不同意”)小霖的观点,因为所有的化学反应都遵循质量守恒定律.
(3)小明同学按如图所示的装置改进实验,验证了质量守恒定律,却发现产物中还有少量淡黄色固体.
[提出问题]淡黄色固体是什么?
[查阅资料]小明同学查阅资料,记录了下列几种含有镁元素的物质的颜色.
其他同学认为不必查阅氯化镁的颜色,理由是空气的成分中不含氯元素;
[提出猜想]分析资料,根据颜色判断,李霖认为该淡黄色固体应该是氮化镁,可能是由镁与空气中的氮气反应生成的,反应的化学方程式为3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2.
[实验探究]小霖设计实验证实了自己的猜想,她的方案可能将点燃的镁条伸人充满氮气的集气瓶中,观察是否生成淡黄色的固体;
[反思与评价]通过上述实验,我们可以发现燃烧不一定需要氧气.
[相关结论]空气中氮气(N2)和氧气(O2)的体积比约为4:1,但镁条在空气中燃烧只生成少量的淡黄色固体,由此得出的一个结论是氮气含量多但是很稳定,难以发生反应.
 某兴趣小组为了验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组为了验证质量守恒定律,做了镁条在空气中燃烧的实验.(1)请写出镁条与氧气反应的化学方程式2Mg+O2 $\frac{\underline{\;点燃\;}}{\;}$2MgO.
(2)小霖发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵守质量守恒定律.我不同意
(填“同意”或“不同意”)小霖的观点,因为所有的化学反应都遵循质量守恒定律.
(3)小明同学按如图所示的装置改进实验,验证了质量守恒定律,却发现产物中还有少量淡黄色固体.
[提出问题]淡黄色固体是什么?
| 物 质 | MgO | MgCl2 | Mg3N2 | Mg(NO3)2 | MgCO3 | Mg(OH)2 |
| 颜 色 | 白色 | 白色 | 淡黄色 | 白色 | 白色 | 白色 |
其他同学认为不必查阅氯化镁的颜色,理由是空气的成分中不含氯元素;
[提出猜想]分析资料,根据颜色判断,李霖认为该淡黄色固体应该是氮化镁,可能是由镁与空气中的氮气反应生成的,反应的化学方程式为3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2.
[实验探究]小霖设计实验证实了自己的猜想,她的方案可能将点燃的镁条伸人充满氮气的集气瓶中,观察是否生成淡黄色的固体;
[反思与评价]通过上述实验,我们可以发现燃烧不一定需要氧气.
[相关结论]空气中氮气(N2)和氧气(O2)的体积比约为4:1,但镁条在空气中燃烧只生成少量的淡黄色固体,由此得出的一个结论是氮气含量多但是很稳定,难以发生反应.