题目内容
11.如图是某密闭容器中物质变化过程的微观示意图(其中“ ”、“
”、“ ”代表不同的原子),下列判断错误的是( )
”代表不同的原子),下列判断错误的是( )
| A. | 变化I只是分子的间隔变大 | B. | 变化Ⅱ是分解反应 | ||
| C. | 丙表示的是混合物 | D. | 化学变化中原子发生了变化 |
分析 根据图示结合已有的知识进行分析解答,一般温度升高时,分子的间隔变大;根据反应的特点分析反应的类型,原子是化学变化中最小的粒子.
解答 解:题目中的微观示意图转化为
则:
A、从图可以看出,变化Ⅰ只是分子的间隔和排列方式发生了改变,说法正确;
B、根据图可知,变化Ⅱ有新物质生成,属于化学变化,并且是由一种物质生成两种或两种以上物质的反应,属于分解反应,说法正确;
C、丙中有三种物质,是混合物,说法正确;
D、化学变化中原子没有发生变化,说法错误.
故选:D.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义进行分析问题、解决问题的能力,同时又用到了物质的构成、物质的变化的知识,属于基础知识的考查.

练习册系列答案
相关题目
1.现将石灰石样品15g与过量的105.4g稀盐酸放入烧杯中充分反应(杂质不与稀盐酸反应),反应时间与反应前后烧杯内物质的质量变化如表所示:
请回答:
(1)完全反应后生成CO2的质量是4.4g.
(2)反应时间为120s时烧杯内溶液中含有的阳离子H+,Ca2+.
(3)计算样品中碳酸钙的质量分数为多少?(计算结果保留一位小数)
| 反应时间/s | 20 | 40 | 60 | 80 | 100 | 120 |
| 质量/g | 119.52 | 118.64 | 117.76 | 116.88 | 116 | 116 |
(1)完全反应后生成CO2的质量是4.4g.
(2)反应时间为120s时烧杯内溶液中含有的阳离子H+,Ca2+.
(3)计算样品中碳酸钙的质量分数为多少?(计算结果保留一位小数)
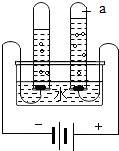
2.回答下列实验的相关问题:
(1)A中试管a中产生的气体是氧气.
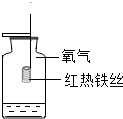
(2)B中发生反应的化学方程式为3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
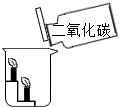
(3)C中观察到的现象是蜡烛自下而上依次熄灭.
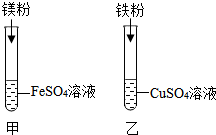
(4)D实验得出的结论是Mg>Fe>Cu.
 |  |  |  |
| A | B | C | D |
(2)B中发生反应的化学方程式为3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
(3)C中观察到的现象是蜡烛自下而上依次熄灭.
(4)D实验得出的结论是Mg>Fe>Cu.
19.将密封良好的袋装食品从平原带到高原时,包装袋会鼓起,是因为袋内的气体分子( )
| A. | 个数增多 | B. | 间隔增大 | C. | 质量增大 | D. | 体积增大 |
16.火星大气层中含有一种称为硫化羰的物质,化学式为COS.已知硫化羰与二氧化碳的结构相似,但能在氧气中完全燃烧.下列有关硫化羰的说法错误的是( )
| A. | 同条件下密度比空气大 | B. | 可作为理想燃料 | ||
| C. | 完全燃烧会生成CO2和SO2 | D. | 不能用作灭火剂 |
20.下列有关化学实验的“目的→操作→现象→结论”的描述都正确的是( )
| 选项 | 目的 | 操作 | 现象 | 结论 |
| A | 比较铝和铜的金 属活动性 | 将一个洁净的铜丝 浸入硫酸铝溶液中 | 无变化 | 铝的金属活动性比铜强 |
| B | 检验露置在空气中的氢氧化钠溶 液是否变质 | 取一定量的氢氧化钠溶液样品,逐滴滴入稀盐酸 | 开始时没有观察到气泡产生 | 氢氧化钠溶液没有变质 |
| C | 探究稀盐酸与氢氧化钠溶液是否恰好完全反应 | 向稀盐酸与氢氧化钠溶液反应所得的溶液中滴加酚酞溶液 | 酚酞溶液仍为无色 | 稀盐酸与氢氧化钠溶液恰好完全反应 |
| D | 检验集气瓶中是否集满二氧化碳 | 将燃烧的木条伸入集 气瓶中 | 燃着的木条立即熄灭 | 集气瓶中已集满二氧化碳 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
1.下列场所挂的图标与“消防安全”不相符的是( )
| A. |  液化气站 | B. |  加油站 | ||
| C. |  图书馆 | D. |  电影院 |