题目内容
15.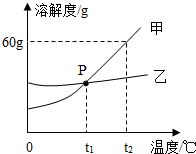 海水中蕴含着80多中元素,海洋是一座巨大的宝库.氯碱工业以海水为原材料可以大量制取烧碱和氯气,它们都是重要的化工生产原料,可以进一步加工成多种化工产品,广泛用于工业生产.所以氯碱工业及相关产品几乎涉及国民经济及人民生活的各个领域.
海水中蕴含着80多中元素,海洋是一座巨大的宝库.氯碱工业以海水为原材料可以大量制取烧碱和氯气,它们都是重要的化工生产原料,可以进一步加工成多种化工产品,广泛用于工业生产.所以氯碱工业及相关产品几乎涉及国民经济及人民生活的各个领域.(1)氯碱工业中发生反应的化学方程式为:2NaCl+2H2O=2NaOH+Cl2↑+A,则A的化学式为H2.
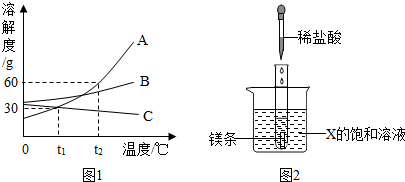
(2)如图是甲、乙两种固体物质的溶解度曲线.
①P点的意义是t1℃时,甲、乙两物质的溶解度相等.
②甲物质中含有少量乙物质,提纯甲物质可用方法降温结晶(选填“降温结晶”、“蒸发结晶”之一).请简述理由甲物质的溶解度随温度的降低而明显减小,而乙物质的溶解度随温度的降低变化不大.
③t2℃时,将50g甲与50g水混合后所得的溶液的质量分数为37.5%.
分析 (1)根据质量守恒定律分析A的化学式;
(2)①根据溶解度曲线交点的意义分析回答;
②根据甲、乙的溶解度随温度变化的情况分析分离提纯的方法;
③根据t2℃时,甲的溶解度的意义分析计算.
解答 解:(1)根据质量守恒定律和氯碱工业中发生反应的化学方程式为:2NaCl+2H2O=2NaOH+Cl2↑+A,反应前有;2Na、2Cl、4H、2O,反应后有:2Na、2H、2Cl、2O,故A中含有两个氢原子,故化学式为:H2;
(2)①P点是t1℃时甲、乙两物质的溶解度曲线的交点,表示的意义是:在t1℃时,甲、乙两物质的溶解度相等;
②从溶解度曲线可以看出:甲物质的溶解度随温度的降低而明显减小,而乙物质的溶解度随温度的降低变化不大,所以甲物质中含有少量乙物质,可采用降温结晶的方法提纯A物质;
③从溶解度曲线可以看出,t2℃时,甲的溶解度为60g,由此可知50g的水中只能溶解30g的甲物质,所以,将50g甲与50g水混合后所得的溶液为饱和溶液,则甲的饱和溶液中溶质的质量分数=$\frac{60g}{100g+60g}$×100%=37.5%.
故答案为:(1)H2;(2)①在t1℃,甲乙两物质溶解度相等;②降温结晶,甲物质的溶解度随温度的降低而明显减小,而乙物质的溶解度随温度的降低变化不大③37.5%.
点评 熟练掌握质量守恒定律及其应用;会读溶解度曲线,并利用它处理题目.

练习册系列答案
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
5. 实验课上,甲同学用石蕊试液测定稀盐酸和NaOH溶液的酸碱性,乙同学用石蕊试液测定石灰水和Na2CO3溶液的酸碱性(如图所示).实验后进行废液处理:甲同学将两支试管中的液体倒入烧杯A中,得到蓝色溶液;乙同学将两支试管中的液体倒入烧杯B中,得到蓝色溶液和白色沉淀;最终将A中的溶液和B中的上层清液倒入烧杯C中.
实验课上,甲同学用石蕊试液测定稀盐酸和NaOH溶液的酸碱性,乙同学用石蕊试液测定石灰水和Na2CO3溶液的酸碱性(如图所示).实验后进行废液处理:甲同学将两支试管中的液体倒入烧杯A中,得到蓝色溶液;乙同学将两支试管中的液体倒入烧杯B中,得到蓝色溶液和白色沉淀;最终将A中的溶液和B中的上层清液倒入烧杯C中.
(1)甲同学的实验中向稀盐酸中滴加石蕊试液后,溶液颜色为红色.
(2)甲同学将两支试管中的液体混合后,烧杯A溶液中的溶质有BC.
A.HClB.NaOHC.NaCl
(3)两位同学继续对烧杯C中的废液成分进行探究:
【猜想与假设】通过分析上述实验现象,烧杯C中的废液除石蕊和水外,其组成可能为:
①NaCl和NaOH,②NaOH、NaCl、Na2CO3,③NaOH、NaCl、Ca(OH)2.
【设计完成实验】请设计实验验证烧杯C中的废液可能的组成:
(4)最后,两位同学向烧杯C中加入适量的稀盐酸,实现了此次实验的绿色排放(呈中性).
 实验课上,甲同学用石蕊试液测定稀盐酸和NaOH溶液的酸碱性,乙同学用石蕊试液测定石灰水和Na2CO3溶液的酸碱性(如图所示).实验后进行废液处理:甲同学将两支试管中的液体倒入烧杯A中,得到蓝色溶液;乙同学将两支试管中的液体倒入烧杯B中,得到蓝色溶液和白色沉淀;最终将A中的溶液和B中的上层清液倒入烧杯C中.
实验课上,甲同学用石蕊试液测定稀盐酸和NaOH溶液的酸碱性,乙同学用石蕊试液测定石灰水和Na2CO3溶液的酸碱性(如图所示).实验后进行废液处理:甲同学将两支试管中的液体倒入烧杯A中,得到蓝色溶液;乙同学将两支试管中的液体倒入烧杯B中,得到蓝色溶液和白色沉淀;最终将A中的溶液和B中的上层清液倒入烧杯C中.(1)甲同学的实验中向稀盐酸中滴加石蕊试液后,溶液颜色为红色.
(2)甲同学将两支试管中的液体混合后,烧杯A溶液中的溶质有BC.
A.HClB.NaOHC.NaCl
(3)两位同学继续对烧杯C中的废液成分进行探究:
【猜想与假设】通过分析上述实验现象,烧杯C中的废液除石蕊和水外,其组成可能为:
①NaCl和NaOH,②NaOH、NaCl、Na2CO3,③NaOH、NaCl、Ca(OH)2.
【设计完成实验】请设计实验验证烧杯C中的废液可能的组成:
| 操作方法 | 实验现象 | 实验结论 |
| ①取少量滤液于试管中,向其中滴加足量的稀盐酸 ②取少量滤液于试管中,向其中加入碳酸钠溶液 ③取两只试管,分别加入少量的滤液,分别滴加足量的稀盐酸和碳酸钠溶液 | 有气泡产生 有沉淀产生 以上两只试管均无现象 | 则C中的废液成分是NaOH、NaCl、Na2CO3 则C中的废液成分是NaOH、NaCl、Ca(OH)2 则C中的废液成分是NaOH、NaCl |
6.下列图象不能正确反映其对应操作的是( )
| A. | 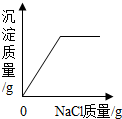 在一定量的AgNO3溶液中逐滴加入NaCl溶液 在一定量的AgNO3溶液中逐滴加入NaCl溶液 | |
| B. | 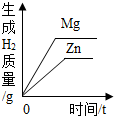 等质量的Zn和Mg分别与等体积等质量分数的稀硫酸(足量)反应 等质量的Zn和Mg分别与等体积等质量分数的稀硫酸(足量)反应 | |
| C. |  向NaOH溶液中逐滴加入稀盐酸 向NaOH溶液中逐滴加入稀盐酸 | |
| D. |  向NaOH和Na2CO3的混合溶液中,逐滴加入稀盐酸 向NaOH和Na2CO3的混合溶液中,逐滴加入稀盐酸 |
10.小吴查阅资料获得有关物质燃烧的新信息:
甲:2Na+Cl2$\frac{\underline{\;点燃\;}}{\;}$2NaCl 乙:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C
并形成以下几点认识:①工业上常用反应甲生产食盐;②燃烧不一定要有氧气参与;
③反应乙属于氧化-还原反应;④使用CO2灭火应有所选择.其中正确的是( )
甲:2Na+Cl2$\frac{\underline{\;点燃\;}}{\;}$2NaCl 乙:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C
并形成以下几点认识:①工业上常用反应甲生产食盐;②燃烧不一定要有氧气参与;
③反应乙属于氧化-还原反应;④使用CO2灭火应有所选择.其中正确的是( )
| A. | 只有①③ | B. | 只有②④ | C. | 只有②③④ | D. | 只有①②④ |
20.下列化学用语正确的是( )
| A. | 硝酸镁-MgNO3 | B. | 2个钾离子-2K+ | C. | 3个氧原子-O3 | D. | 氧化铝-AlO |
7.下列物质由原子直接构成的是( )
| A. | NaCl | B. | H2O | C. | CO2 | D. | Fe |
 江西不仅山清水秀、景色迷人,特色美食更是遍布各地令各路“吃货”流连忘返.
江西不仅山清水秀、景色迷人,特色美食更是遍布各地令各路“吃货”流连忘返.