题目内容
8.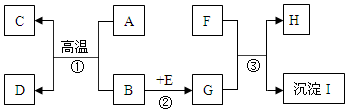 A~I是初中化学常见的物质,他们之间的相互关系如图所示,其中B是红色固体,A、C常温下是气体.请回答下面问题:
A~I是初中化学常见的物质,他们之间的相互关系如图所示,其中B是红色固体,A、C常温下是气体.请回答下面问题:(1)物质C的化学式是CO2;
(2)若H为氯化钠,反应③的化学方程式为3NaOH+FeCl3═Fe(OH)3↓+3NaCl,基本类型为复分解反应.
(3)若H和I中含有一种相同的元素,且H为不溶于稀硝酸的白色沉淀,反应②的方程式为Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
分析 根据A~I是初中化学常见的物质,B是红色粉末,A、C常温下是气体,A和B高温会生成C和D,所以A是一氧化碳,B是氧化铁,氧化铁和一氧化碳高温生成铁和二氧化碳,所以C是二氧化碳,D是铁,氧化铁和E生成的G和F会生成不溶于硝酸的沉淀H,故H可能是硫酸钡,G可能是硫酸铁,然后将推出的物质进行验证即可.
解答 解:(1)B是红色粉末,A、C常温下是气体,A和B高温会生成C和D,所以A是一氧化碳,B是氧化铁,氧化铁和一氧化碳高温生成铁和二氧化碳,所以C是二氧化碳,D是铁,故C是二氧化碳,故填:CO2;
(2)若H是氯化钠,则E可能是盐酸,盐酸与氧化铁反应生成氯化铁和水,氯化铁与氢氧化钠反应生成氢氧化铁沉淀和氯化钠,故反应③是氢氧化钠与氯化铁的反应,属于复分解反应,故填:3NaOH+FeCl3═Fe(OH)3↓+3NaCl;复分解反应;
(3)H和I中含有一种相同的元素,且H为不溶于稀硝酸的白色沉淀,则H可能是硫酸钡,E是硫酸,硫酸与氧化铁反应生成硫酸铁和水,硫酸铁与氢氧化钡反应生成氢氧化铁沉淀和硫酸钡,含有相同的氧元素,故反应②是氧化铁与硫酸的反应,故填:Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
相关题目
18.下列说法中,没有错误的是( )
| A. | 一氧化碳与二氧化碳都是由碳元素组成的,所以它们的化学性质相同 | |
| B. | 金刚石和石墨里碳原子的排列不同,因此,它们的物理性质有很大的差别 | |
| C. | 二氧化碳通入石蕊试液中变红,是二氧化碳使石蕊试液变红 | |
| D. | 二氧化碳不支持燃烧,所有的物质着火燃烧都能用二氧化碳来灭火 |
16.下列是某同学鉴别二氧化碳和一氧化碳的方法,其中不正确的是( )
| A | B | C | D | |
| 实验 方案 | 通过灼热的氧化铜 | 用燃烧的木条分别伸入集气瓶中 | 将气体分别通人盛水的烧杯中 | 将气体分别通人澄清石灰水中 |
| A. | A | B. | B | C. | C | D. | D |
17. 甲烷和水反应可以制备水煤气(混合气体),其反应的微观示意图如图所示,根据微观示意图得出的结论中,正确的是( )
甲烷和水反应可以制备水煤气(混合气体),其反应的微观示意图如图所示,根据微观示意图得出的结论中,正确的是( )
 甲烷和水反应可以制备水煤气(混合气体),其反应的微观示意图如图所示,根据微观示意图得出的结论中,正确的是( )
甲烷和水反应可以制备水煤气(混合气体),其反应的微观示意图如图所示,根据微观示意图得出的结论中,正确的是( )| A. | 反应前后碳元素化合价没有发生变化 | |
| B. | 反应中甲和丙的质量之比为4:7 | |
| C. | 水煤气的成分是一氧化碳和氧气 | |
| D. | 反应中含氢元素的化合物有三种 |
18.甲、乙两种固体物质的溶解度曲线如图所示,下列叙述中正确的是( )


| A. | 甲物质的溶解度大于乙物质的溶解度 | |
| B. | t2℃时,将30g甲物质放入70g水中,所得饱和溶液的质量为100g | |
| C. | t1℃时,甲、乙两物质的溶解度相等 | |
| D. | 甲溶液从t2℃降温到t1℃,一定有晶体析出 |

 已知D为黑色粉末,B、C为气体,A为红色固体.A、B、C、D、E五种物质之间的转化关系如图所示.请回答:
已知D为黑色粉末,B、C为气体,A为红色固体.A、B、C、D、E五种物质之间的转化关系如图所示.请回答: