题目内容
18.甲、乙两种固体物质的溶解度曲线如图所示,下列叙述中正确的是( )
| A. | 甲物质的溶解度大于乙物质的溶解度 | |
| B. | t2℃时,将30g甲物质放入70g水中,所得饱和溶液的质量为100g | |
| C. | t1℃时,甲、乙两物质的溶解度相等 | |
| D. | 甲溶液从t2℃降温到t1℃,一定有晶体析出 |
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:A、在比较物质的溶解度时,需要指明温度,故A错误;
B、t2℃时,甲物质的溶解度是30g,所以将30g甲物质放入70g水中,所得饱和溶液的质量为91g,故B错误;
C、通过分析溶解度曲线可知,t1℃时,甲、乙两物质的溶解度相等,故C正确;
D、甲溶液的状态不确定,所以甲溶液从t2℃降温到t1℃,不一定有晶体析出,故D错误.
故选:C.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
9.下列图示实验操作中,正确的是( )
| A. | 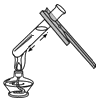 | B. | 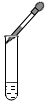 | C. |  | D. | 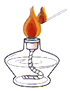 |
6.建立基本的化学观念可以让我们更好的理解化学,如形成守恒观念,可以更好的理解质量守恒定律,下列表述正确的是( )
| A. | 每1个C原子和1个O2分子反应,生成2个CO2分子 | |
| B. | 32g S与32g O2完全反应,生成64g SO2 | |
| C. | 镁条燃烧后固体质量增加,故质量守恒定律不是普遍规律 | |
| D. | 10g水蒸气变成10g水蒸气,变化前后质量相等,遵循质量守恒定律 |
13.下列说法错误的是( )
| A. | 生铁和钢都是铁合金 | |
| B. | 金刚石和石墨都是由碳元素组成的单质 | |
| C. | 空气和液氧都是混合物 | |
| D. | NO2和Fe2O3都是氧化物 |
3.现有甲、乙、丙、丁四种颗粒大小相同的金属,分别投入相同的稀硫酸中,只有甲、乙表面有气泡产生,且甲产生气泡较快;再把丙和丁投入相同的硝酸银溶液中,过一会儿,丙的表面有银析出,而丁没变化,则四种金属的活动性顺序是( )
| A. | 甲>乙>丙>丁 | B. | 丁>乙>丙>甲 | C. | 丙>乙>丁>甲 | D. | 乙>甲>丁>丙 |
10. 某反应的微观示意图如图,用“
某反应的微观示意图如图,用“ ”与“
”与“ ”代表A、B两种元素的原子.下列说法不正确的是( )
”代表A、B两种元素的原子.下列说法不正确的是( )
 某反应的微观示意图如图,用“
某反应的微观示意图如图,用“ ”与“
”与“ ”代表A、B两种元素的原子.下列说法不正确的是( )
”代表A、B两种元素的原子.下列说法不正确的是( )| A. | 该反应属于化合反应 | |
| B. | 反应前后原子的种类不发生变化 | |
| C. | 反应前后物质的化学性质不发生变化 | |
| D. | 该反应的化学方程式表示为A2+3B2═2AB3 |
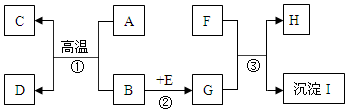 A~I是初中化学常见的物质,他们之间的相互关系如图所示,其中B是红色固体,A、C常温下是气体.请回答下面问题:
A~I是初中化学常见的物质,他们之间的相互关系如图所示,其中B是红色固体,A、C常温下是气体.请回答下面问题: 金属材料在生活、生产中应用十分广泛.
金属材料在生活、生产中应用十分广泛.