题目内容
KNO3和KCl在不同温度时的溶解度如下表所示,请回答下列问题:| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
| 溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
| KCl | 27.6 | 31.0 | 34.6 | 37 | 40.0 | 42.6 | 45.5 | 48.3 | |
(2)10℃时,将50g溶质质量分数为10%的KCl溶液配制为质量分数为5%的溶液,加水质量为 g.
(3)根据溶解度曲线可以知道,若从m的饱和溶液中析出晶体,应该采用 结晶的方法.
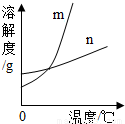
【答案】分析:(1)根据0℃时两物质的溶解度判断
(2)根据加水稀释前后溶质质量不变解答
(3)根据结晶方法分析
解答:解:(1)依据上表数据可知0℃时硝酸钾的溶解度小于氯化钾的溶解度,因此图中m能表示KNO3溶解度曲线.
(2)设加水的质量为x,根据加水稀释前后溶质质量不变可得
50g×10%=(50g+x)×5% x=50g
(3)根据溶解度曲线可以知道,m的溶解度受温度影响较大,因此若从m的饱和溶液中析出晶体,应该采用降温结晶的方法
故答案为:(1)m(2)50(3)降温
点评:本题考查溶解度表格与图象的结合,溶液稀释计算以及结晶的方法,属于基本题型的考查.
(2)根据加水稀释前后溶质质量不变解答
(3)根据结晶方法分析
解答:解:(1)依据上表数据可知0℃时硝酸钾的溶解度小于氯化钾的溶解度,因此图中m能表示KNO3溶解度曲线.
(2)设加水的质量为x,根据加水稀释前后溶质质量不变可得
50g×10%=(50g+x)×5% x=50g
(3)根据溶解度曲线可以知道,m的溶解度受温度影响较大,因此若从m的饱和溶液中析出晶体,应该采用降温结晶的方法
故答案为:(1)m(2)50(3)降温
点评:本题考查溶解度表格与图象的结合,溶液稀释计算以及结晶的方法,属于基本题型的考查.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 KNO3和KCl在不同温度时的溶解度如下表所示.
KNO3和KCl在不同温度时的溶解度如下表所示. (2013?河东区二模)KNO3和KCl在不同温度时的溶解度如表所示.请回答下列问题:
(2013?河东区二模)KNO3和KCl在不同温度时的溶解度如表所示.请回答下列问题: KNO3和KCl在不同温度时的溶解度如下表所示.请回答下列问题:
KNO3和KCl在不同温度时的溶解度如下表所示.请回答下列问题: KNO3和KCl在不同温度时的溶解度如下表所示.
KNO3和KCl在不同温度时的溶解度如下表所示.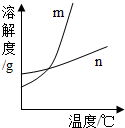 KNO3和KCl在不同温度时的溶解度如下表所示.请回答下列问题:
KNO3和KCl在不同温度时的溶解度如下表所示.请回答下列问题: