题目内容
18.下列对应关系错误的是( )| A. | 氧气──供人呼吸 | B. | 二氧化碳──造成酸雨 | ||
| C. | 氮气──作保护气 | D. | 氙──医疗麻醉 |
分析 A、根据氧气化学性质活泼分析;
B、根据造成酸雨的气体分析;
C、根据氮气的性质分析;
D、从氙气能抑制人体神经,可用于医疗麻醉去分析.
解答 解:A、氧气支持呼吸,可供人呼吸,故A正确;
B、造成酸雨的气体主要是由化石燃料燃烧产生的二氧化硫、氮氧化物等酸性气体,经过复杂的大气化学反应,被雨水吸收溶解而成.故B错误;
C、氮气化学性质稳定,常用做保护气,故C正确;
D、氙气能抑制人体神经,可用于医疗麻醉,故D正确..
故选:B.
点评 酸雨对环境的危害已经是较为严重的环境问题,受到社会越来越多的关注,同时也是中考的重要考题之一.

练习册系列答案
相关题目
8.有两瓶体积相同的溶液,一瓶为浓硫酸,另一瓶为稀硫酸,下列方法,不能用来区别它们的是( )
| A. | 看外观 | |
| B. | 分别加入到少量水中,观察温度的变化 | |
| C. | 分别称量 | |
| D. | 分别用小木条蘸取少量,观察木条是否变黑 |
9.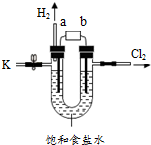 某学习小组在老师的指导下,用自制的实验装置(如图所示)进行电解饱和食盐水的实验.
某学习小组在老师的指导下,用自制的实验装置(如图所示)进行电解饱和食盐水的实验.
资料:
1:电解饱和食盐水的化学方程式:
2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$ 2NaOH+H2↑+Cl2↑
2:Cl2能溶于水.
探究活动一:确定电解饱和食盐水后的产物
(1)此电解原理与电解水原理类似,则a端为电源的负
极,甲组同学为了收集另一电极产生的气体,
他们用向上排空气法 法进行收集;
(2)甲组同学从K处取出一部分待测液,往里面加入
酚酞,发现溶液变红,说明电解后生成了氢氧化钠;
探究活动二:测定待测液中氢氧化钠的质量分数
【实验1】用酸碱中和法测定
甲组同学称取10g待测液于烧杯中,加水稀释,用带有刻度的滴管逐滴加入溶质质量分数为19.6%的稀硫酸,边加边振荡,用pH计测定溶液的pH,所得数据如下:
(3)写出氢氧化钠与稀硫酸反应的化学方程式:2NaOH+H2SO4=Na2SO4+2H2O;
(4)当加入6g稀硫酸时,溶液中溶质为氢氧化钠、硫酸钠,利用氢氧化钠与稀硫酸恰好完全反应时的实验数据,计算待测液中氢氧化钠的质量分数为16%;
【实验2】用沉淀法测定
资料摘要:氢氧化钠与氯化镁溶液发生反应:2NaOH+MgCl2=Mg(OH)2↓+2NaCl
乙组同学按下图所示的实验步骤进行实验:

(5)步骤 ②加入的氯化镁溶液必须足量,其目的是使氢氧化钠完全反应;滴加一定量氯化镁溶液后,判断所加氯化镁溶液是否足量的具体操作:静置,取少量反应后的待测溶液,滴加氢氧化钠;产生白色沉淀,氯化镁已经过量(写出实验步骤、现象和结论);
(6)步骤 ③过滤出的沉淀物是氢氧化镁(填物质的名称);
(7)利用沉淀物的质量计算氢氧化钠的质量分数,若缺少步骤④的操作,所
测定氢氧化钠的质量分数将偏大(选填“偏大”、“偏小”或“没影响”).
 某学习小组在老师的指导下,用自制的实验装置(如图所示)进行电解饱和食盐水的实验.
某学习小组在老师的指导下,用自制的实验装置(如图所示)进行电解饱和食盐水的实验.资料:
1:电解饱和食盐水的化学方程式:
2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$ 2NaOH+H2↑+Cl2↑
2:Cl2能溶于水.
探究活动一:确定电解饱和食盐水后的产物
(1)此电解原理与电解水原理类似,则a端为电源的负
极,甲组同学为了收集另一电极产生的气体,
他们用向上排空气法 法进行收集;
(2)甲组同学从K处取出一部分待测液,往里面加入
酚酞,发现溶液变红,说明电解后生成了氢氧化钠;
探究活动二:测定待测液中氢氧化钠的质量分数
【实验1】用酸碱中和法测定
甲组同学称取10g待测液于烧杯中,加水稀释,用带有刻度的滴管逐滴加入溶质质量分数为19.6%的稀硫酸,边加边振荡,用pH计测定溶液的pH,所得数据如下:
| 加入稀硫酸的质量/g | 0 | 4.0 | 6.0 | 8.0 | 10.0 | 12.0 |
| 烧杯中溶液的pH | 13.0 | 12.8 | 12.5 | 12.3 | 7.0 | 1.3 |
(4)当加入6g稀硫酸时,溶液中溶质为氢氧化钠、硫酸钠,利用氢氧化钠与稀硫酸恰好完全反应时的实验数据,计算待测液中氢氧化钠的质量分数为16%;
【实验2】用沉淀法测定
资料摘要:氢氧化钠与氯化镁溶液发生反应:2NaOH+MgCl2=Mg(OH)2↓+2NaCl
乙组同学按下图所示的实验步骤进行实验:

(5)步骤 ②加入的氯化镁溶液必须足量,其目的是使氢氧化钠完全反应;滴加一定量氯化镁溶液后,判断所加氯化镁溶液是否足量的具体操作:静置,取少量反应后的待测溶液,滴加氢氧化钠;产生白色沉淀,氯化镁已经过量(写出实验步骤、现象和结论);
(6)步骤 ③过滤出的沉淀物是氢氧化镁(填物质的名称);
(7)利用沉淀物的质量计算氢氧化钠的质量分数,若缺少步骤④的操作,所
测定氢氧化钠的质量分数将偏大(选填“偏大”、“偏小”或“没影响”).
6.以下做法错误的是( )
| A. | 使用乙醇汽油,可适当节省石油资源,并能避免汽车尾气的污染 | |
| B. | 塑料长期堆积既破坏土壤又污染地下水,应将塑料制品分类回收,可有效缓解“白色污染” | |
| C. | 进入久未开启的菜窖之前,应先进行灯火实验 | |
| D. | 一方面植树、造林、种草,另一方面利用和开发太阳能、核能等新能源,能有效抑制温室效应 |
3.下列叙述中属于食盐用途的是( )
①日常烹饪中作调味品
②重要的化工原料如制造氢氧化钠
③制盐酸
④腌制食品.
①日常烹饪中作调味品
②重要的化工原料如制造氢氧化钠
③制盐酸
④腌制食品.
| A. | ①② | B. | ①④ | C. | ①②④ | D. | 全部 |
10.下列说法中正确的是( )
| A. | 具有相同质子数的微粒一定属于同一种元素 | |
| B. | 由不同种元素组成的物质一定是化合物 | |
| C. | 盐的组成元素中一定不含氢元素 | |
| D. | 不饱和溶液变成饱和溶液后溶质的质量分数可能不变 |
8.缺乏科学常识而造成伤亡事故时有发生.下列做法正确的是( )
| A. | 将亚硝酸盐当食盐食用 | |
| B. | 电器失火时,先用水灭火 | |
| C. | 不接触高于安全电压的低压带电体,不靠近高压带电体 | |
| D. | 有金属外壳的家用电器,其外壳的接地线要接在电源的零线上 |
 用五个圆A、B、C、D、E分别表示五种物质,他们之间反应关系如右图所示.溶液A是胃酸的成分,B可用于造纸、纺织等工业,溶液A与溶液B能发生中和反应,C、D、E、分别是三种氧化物,D能和E 反应制得熟石灰,C是空气的组成成分之一.请利用初中化学知识回答下列问题:
用五个圆A、B、C、D、E分别表示五种物质,他们之间反应关系如右图所示.溶液A是胃酸的成分,B可用于造纸、纺织等工业,溶液A与溶液B能发生中和反应,C、D、E、分别是三种氧化物,D能和E 反应制得熟石灰,C是空气的组成成分之一.请利用初中化学知识回答下列问题: