题目内容
9.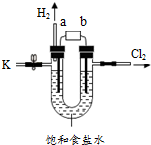 某学习小组在老师的指导下,用自制的实验装置(如图所示)进行电解饱和食盐水的实验.
某学习小组在老师的指导下,用自制的实验装置(如图所示)进行电解饱和食盐水的实验.资料:
1:电解饱和食盐水的化学方程式:
2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$ 2NaOH+H2↑+Cl2↑
2:Cl2能溶于水.
探究活动一:确定电解饱和食盐水后的产物
(1)此电解原理与电解水原理类似,则a端为电源的负
极,甲组同学为了收集另一电极产生的气体,
他们用向上排空气法 法进行收集;
(2)甲组同学从K处取出一部分待测液,往里面加入
酚酞,发现溶液变红,说明电解后生成了氢氧化钠;
探究活动二:测定待测液中氢氧化钠的质量分数
【实验1】用酸碱中和法测定
甲组同学称取10g待测液于烧杯中,加水稀释,用带有刻度的滴管逐滴加入溶质质量分数为19.6%的稀硫酸,边加边振荡,用pH计测定溶液的pH,所得数据如下:
| 加入稀硫酸的质量/g | 0 | 4.0 | 6.0 | 8.0 | 10.0 | 12.0 |
| 烧杯中溶液的pH | 13.0 | 12.8 | 12.5 | 12.3 | 7.0 | 1.3 |
(4)当加入6g稀硫酸时,溶液中溶质为氢氧化钠、硫酸钠,利用氢氧化钠与稀硫酸恰好完全反应时的实验数据,计算待测液中氢氧化钠的质量分数为16%;
【实验2】用沉淀法测定
资料摘要:氢氧化钠与氯化镁溶液发生反应:2NaOH+MgCl2=Mg(OH)2↓+2NaCl
乙组同学按下图所示的实验步骤进行实验:

(5)步骤 ②加入的氯化镁溶液必须足量,其目的是使氢氧化钠完全反应;滴加一定量氯化镁溶液后,判断所加氯化镁溶液是否足量的具体操作:静置,取少量反应后的待测溶液,滴加氢氧化钠;产生白色沉淀,氯化镁已经过量(写出实验步骤、现象和结论);
(6)步骤 ③过滤出的沉淀物是氢氧化镁(填物质的名称);
(7)利用沉淀物的质量计算氢氧化钠的质量分数,若缺少步骤④的操作,所
测定氢氧化钠的质量分数将偏大(选填“偏大”、“偏小”或“没影响”).
分析 (1)根据同性相斥,异性相吸进行分析;
根据气体的密度和溶解性确定气体的收集方法;
(2)根据碱性物质能使酚酞变红色进行分析;
(3)根据氢氧化钠和硫酸反应生成硫酸钠和水进行分析;
(4)根据加入6g稀硫酸时,溶液的pH值,以及氢氧化钠和硫酸反应会生成硫酸钠进行分析;
根据氢氧化钠和硫酸反应生成硫酸钠和水,以及溶液pH值恰好是7时,所滴加的硫酸的质量进行计算;
(5)根据使氢氧化钠溶液中的氢氧化钠和氯化镁完全反应,氯化镁溶液应该是足量的进行分析;
(6)根据氢氧化钠和氯化镁反应生成氢氧化镁沉淀和氯化钠,因此步骤③过滤出的沉淀物是氢氧化镁进行分析;
(7)根据沉淀物的质量计算氢氧化钠的质量分数时,若不洗涤沉淀,那么沉淀上会附着一些杂质,从而使沉淀的质量增大,会导致计算出的氢氧化钠质量偏大,使所测定氢氧化钠的质量分数偏大进行分析.
解答 解:(1)根据饱和食盐水的点解方程式可知,氢在水中显示正价,带正电荷,所以会向负极运动,氯离子带负电荷,会向正极运动,所以a端为电源的负极,得到氢气,甲组同学为了收集另一电极产生的气体氯气,氯气能溶于水,密度比空气大,所以用向上排空气法进行收集;
(2)碱性物质能使酚酞变红色,依据质量守恒定律可知,往里面加入酚酞,发现溶液变红,说明电解后生成了氢氧化钠;
(3)氢氧化钠和硫酸反应生成硫酸钠和水,化学方程式为:2NaOH+H2SO4=Na2SO4+2H2O;
(4)加入6g稀硫酸时,溶液的pH值是12.5,所以溶液显碱性,溶液中还有氢氧化钠,以及氢氧化钠和硫酸反应会生成硫酸钠,所以当加入6g稀硫酸时,溶液中溶质为氢氧化钠、硫酸钠;
设参加反应的氢氧化钠质量为x,
2NaOH+H2SO4=Na2SO4+2H2O
80 98
x 10g×19.6%
$\frac{80}{x}$=$\frac{98}{10g×19.6%}$
x=1.6g
所以待测液中氢氧化钠的质量分数为:$\frac{1.6g}{10g}$×100%=16%;
(5)步骤②加入的氯化镁溶液必需足量,其目的是使氢氧化钠完全反应;
滴加一定量氯化镁溶液后,判断所加氯化镁溶液是否足量的具体操作:静置,取上层清液于试管中,向试管中滴加氢氧化钠溶液,产生白色沉淀,氯化镁已经过量;
(6)通过推导可知,步骤③过滤出的沉淀物是氢氧化镁;
(7)利用沉淀物的质量计算氢氧化钠的质量分数,若缺少步骤④的操作,沉淀中因含有其他杂质而质量偏大,所测定氢氧化钠的质量分数将偏大.
故答案为:(1)负极,向上排空气法;
(2)氢氧化钠;
(3)2NaOH+H2SO4=Na2SO4+2H2O;
(4)氢氧化钠、硫酸钠;
所以待测液中氢氧化钠的质量分数为:16%;
(5)使氢氧化钠完全反应;
取上层清液于试管中,向试管中滴加氢氧化钠溶液;产生白色沉淀,氯化镁已经过量;
(6)氢氧化镁;
(7)偏大.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

| A. | 加入适量的石灰石粉末 | B. | 加入适量的稀硫酸 | ||
| C. | 通入适量的二氧化碳气体 | D. | 加入适量的酸性废水 |
| A. | 实验室将废液直接倒入下水道 | |
| B. | 实验中未说明药品用量时,取用较多量药品进行实验 | |
| C. | 对废旧电池作深埋处理,消除其污染 | |
| D. | 化工生产中使原料尽可能地转化为产品 |
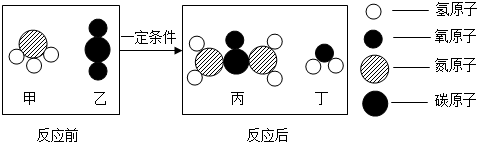
| A. | 甲的化学式为NH3 | B. | 乙、丙、丁都是氧化物 | ||
| C. | 丙中氮、氢元素质量比为2:4 | D. | 参加反应的甲、乙质量比为17:44 |
【知识回放】
金属活动性顺序:K Ca Na Mg Al ZnFeSn Pb(H)CuHg Ag Pt Au,请你
在横线上填写对应金属的元素符号.
【作出猜想】
猜想1.Cr>Fe>Cu;
猜想2.Fe>Cu>Cr;
猜想3.还有可能是Fe>Cr>Cu.
【查阅资料】
(1)铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
(2)铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
【设计与实验】
小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的
同种稀硫酸.
【结论与解释】
| 实验 | 试管1 | 试管2 | 试管3 |
| 实验 操作 |  |  |  |
| 实验 现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变成为蓝色 | 无明显现象发生 |
(2)实验前用砂纸打磨金属片的目的是除去金属表面的氧化膜,利于反应.
【知识运用】
将铬片投入FeSO4溶液中,反应能(填“能”或“不能”)进行.若不能进行,请说明理由;若能进行,请你写出反应的化学方程式Cr+FeSO4=Fe+CrSO4.
| A. | 氧气──供人呼吸 | B. | 二氧化碳──造成酸雨 | ||
| C. | 氮气──作保护气 | D. | 氙──医疗麻醉 |
 将某氢氧化钠溶液逐滴滴入盐酸和氯化铜的混合溶液中,直至过量.根据实验事实绘制如图所示曲线,其中说法正确的是( )
将某氢氧化钠溶液逐滴滴入盐酸和氯化铜的混合溶液中,直至过量.根据实验事实绘制如图所示曲线,其中说法正确的是( )| A. | a至b段有蓝色沉淀生成 | B. | a至d段氯化钠质量不断增大 | ||
| C. | c点比a点所含的溶质种类少 | D. | c至d段,溶液pH不断减小 |
