题目内容
2.烧杯中装有碳酸钠与氯化钠的固体混合物24.4g,先加入80g水完全溶解,再加入100g稀盐酸,完全反应后,共收集到气体4.4g,求完全反应后所得溶液中溶质质量分数.(Na-23 C-12 O-16 H-1 Cl-35.5).分析 根据碳酸钠能与盐酸生成二氧化碳的反应原理对该问题进行分析探讨即可.
解答 解:设该反应生成的氯化钠的质量是x,反应的碳酸钠的质量为y
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 117 44
y x 4.4g
$\frac{106}{y}=\frac{117}{x}=\frac{44}{4.4g}$
x=11.7g,y=10.6g
完全反应后所得溶液中溶质质量分数:$\frac{24.4g-10.6g+11.7g}{24.4g+100g-4.4g}×100%$=21.25%
答:完全反应后所得溶液中溶质质量分数为21.25%.
点评 此题是对化学方程式计算和溶质质量分数有关问题的考查,掌握有关的化学反应的情况判断出气体是二氧化碳是解题的关键.

练习册系列答案
相关题目
7.下列图示是实验的基本操作,其中正确的是( )
| A. |  熄灭酒精灯 | B. | 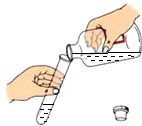 倾倒液体 | C. | 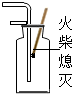 气体验满 | D. | 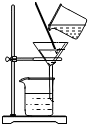 液体过滤 |
12.将同种稀硫酸80g分8次加入10g镁条中(该镁条只含两种物质),测得实验数据见表:
(1)当加入稀硫酸的质量小于20g时没有气体产生,说明的问题是由于镁易于空气中的氧气反应在镁条的表面生成了氧化镁,稀硫酸首先与镁条表面的氧化镁薄膜发生了反应,所以不产生氢气,反应的方程式是:MgO+H2SO4=MgSO4+H2O..
(2)请计算:①10g该镁条中含镁的质量;②若加入20g稀硫酸后立即开始产生气体,求实验所用稀硫酸中溶质的质量分数.
| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | 第6次 | 第7次 | 第8次 | |
| 稀硫酸的质量/g | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 生成气体的质量/g | 0 | 0 | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.5 |
(2)请计算:①10g该镁条中含镁的质量;②若加入20g稀硫酸后立即开始产生气体,求实验所用稀硫酸中溶质的质量分数.
14.下列造成空气污染的因素主要由物理变化引起的是( )
| A. | 生活垃圾焚烧产生的有害气体 | B. | 建筑施工导致尘土飞扬 | ||
| C. | 生物腐烂放出的一氧化碳 | D. | 煤燃烧产生的刺激性气味气体 |
12.下列关于能源的说法中正确的是( )
| A. | 天然气属于可再生能源 | |
| B. | 煤炭、石油都属于不可再生能源 | |
| C. | 原子弹利用的是核裂变,氢弹利用的是核聚变 | |
| D. | 核电站利用核能发电,核反应堆中发生的链式反应是可控的 |

 水是生命之源,“珍惜水、节约水、保护水”是每个公民的义务和责任.
水是生命之源,“珍惜水、节约水、保护水”是每个公民的义务和责任.