题目内容
5.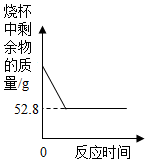 某兴趣小组为了测定鸡蛋壳(主要成分是碳酸钙)中碳酸钙的含量,现取7.8g鸡蛋壳,捣碎,放在烧杯中,然后向其中加入47.2g某浓度的稀盐酸,恰好完全反应(鸡蛋壳中除碳酸钙外,其他成分不与稀盐酸反应也不溶于水),测得烧杯中的反应剩余物的质量与反应时间的关系如图所示(忽略水分的蒸发).
某兴趣小组为了测定鸡蛋壳(主要成分是碳酸钙)中碳酸钙的含量,现取7.8g鸡蛋壳,捣碎,放在烧杯中,然后向其中加入47.2g某浓度的稀盐酸,恰好完全反应(鸡蛋壳中除碳酸钙外,其他成分不与稀盐酸反应也不溶于水),测得烧杯中的反应剩余物的质量与反应时间的关系如图所示(忽略水分的蒸发).求:(1)产生CO2的质量为多少?
(2)该鸡蛋壳中碳酸钙的质量?
(3)反应后所得溶液的质量分数?
分析 根据质量守恒定律可知,过程中质量的减少是因为生成了二氧化碳,所以可以求算二氧化碳的质量,根据二氧化碳和对应的化学方程式求算碳酸钙和氯化钙的质量,进而求算对应的质量分数.
解答 解:根据质量守恒定律可得,生成的二氧化碳的质量为7.8g+47.2g-52.8g=2.2g
设该石灰石样品中碳酸钙的质量为x,生成氯化钙的质量为y
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 111 44
x y 2.2g
$\frac{100}{x}$=$\frac{111}{y}$=$\frac{44}{2.2g}$
x=5g
y=5.55g
反应后所得溶液的质量分数为$\frac{5.55g}{52.8g-(7.8g-5g)}$×100%=11.1%
答:(1)产生CO2的质量为2.2g;
(2)该鸡蛋壳中碳酸钙的质量为5g;
(3)反应后所得溶液的质量分数为11.1%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
15.在给定条件下,下列转化不能一步实现的组合是( )
| A. | Na2CO3$\stackrel{Ba(NO_{3})_{2}}{→}$BaCO3 $\stackrel{CaCl_{2}}{→}$BaSO4 | |
| B. | Cu $→_{△}^{O_{2}}$CuO$\stackrel{H_{2}SO_{4}}{→}$CuSO4 | |
| C. | CaO$\stackrel{H_{2}O}{→}$Ca(OH)2$\stackrel{Na_{2}CO_{3}}{→}$NaOH | |
| D. | CH4$→_{点燃}^{O_{2}}$CO2$→_{点燃}^{Mg}$C |

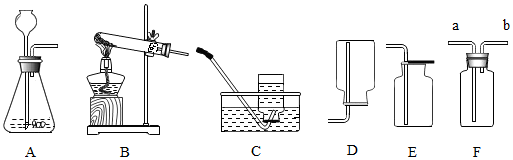

 水和溶液在生活中具有重要用途.
水和溶液在生活中具有重要用途.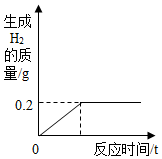 生活中常见的铁制品大多为铁合金(成分为铁和碳)材料,而非纯铁,铁合金又因其含碳量不同分为生铁和钢(生铁含碳量为2%-4.3%,钢含碳量为0.03%-2%).将一块质量为5.8g的铁合金放入烧杯中,再向烧杯中加入98g稀硫酸,反应关系如图所示:通过计算回答:该铁合金是生铁还是钢?(写出计算过程,结果精确到0.1%)
生活中常见的铁制品大多为铁合金(成分为铁和碳)材料,而非纯铁,铁合金又因其含碳量不同分为生铁和钢(生铁含碳量为2%-4.3%,钢含碳量为0.03%-2%).将一块质量为5.8g的铁合金放入烧杯中,再向烧杯中加入98g稀硫酸,反应关系如图所示:通过计算回答:该铁合金是生铁还是钢?(写出计算过程,结果精确到0.1%)