题目内容
18.已知碳酸钙与氯化钙的混合物共重10.9克,加入93.5克稀盐酸恰好完全反应,称得反应后溶液的质量为100克.(1)生成二氧化碳4.4克.
(2)求反应后溶液中溶质的质量分数.
分析 (1)根据质量守恒定律,生成二氧化碳的质量等于氯化钙和碳酸钙的混合物的质量加上稀盐酸的质量减去反应后剩余物质的总质量;
(2)根据化学方程式利用生成的二氧化碳的质量计算出混合物中碳酸钙的质量和生成的氯化钙的质量,溶质有两部分,一是生成的氯化钙,一是原混合物中的氯化钙,原混合物中的氯化钙可以用混合物的质量减去碳酸钙的质量获得,最后利用质量分数公式计算即可.
解答 解:(1)根据质量守恒定律,生成二氧化碳的质量=10.9g+93.5g-100g=4.4g;故填:4.4;
(2)设原混合物中含有碳酸钙的质量为x,生成氯化钙的质量为y,则
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 111 44
x y 4.4g
$\frac{100}{x}=\frac{111}{y}=\frac{44}{4.4g}$
x=10g,y=11.1g
反应后溶液中溶质的质量分数:$\frac{10.9g-10g+11.1g}{100g}×100%$=12%
答:反应后溶液中溶质的质量分数为12%.
点评 本题难度较大,主要考查了以化学方程式计算为基础,同时融入溶液等方面的计算题,这样的题目一直是中考的热点,主要培养学生的综合分析能力和计算能力.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
6.下列变化中既有物理变化又有化学变化的是( )
| A. | 干冰升华 | B. | 点灯发光 | C. | 蜡烛成灰 | D. | 铁铸成锅 |
13.在一密闭容器中,有甲、乙、丙、丁四种物质,在一定的条件下,充分反应,测得反应前后各物质质量如下表,关于此反应,下列认识错误的是( )
| 物 质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量(g) | 4 | 1 | 42 | 10 |
| 反应后质量(g) | X | 20 | 6 | 10 |
| A. | X的值为0 | |
| B. | 参加反应的甲、丙的质量比为1:9 | |
| C. | 乙、丁的相对分子质量比一定为19:21 | |
| D. | 该反应的反应类型一定不是化合反应 |
10.某同学为了探究盐酸的性质,已经用了①紫色石蕊试剂和酚酞,②Fe和Zn,③CuO和Fe2O3,④CaCO3和AgNO3四组药品分别跟盐酸反应.为了更全面了解盐酸的性质,他还应选下列哪一组药品( )
| A. | Mg和Al | B. | NaOH和Ca(OH)2 | C. | Na2CO3和K2CO3 | D. | MgO和Al2O3 |
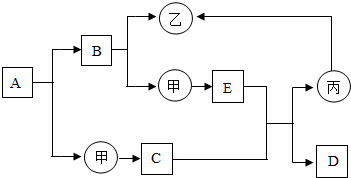 如图是初中化学中常见物质间的转化关系,其中甲、乙、丙为单质;A、B、C、D、E为同类化合物,且A与B的组成元素相同,D与E的组成元素也相同.已知C为红色固体、丙为黑色粉末,C和E在高温条件下可生成丙和D,D能使澄清的石灰水变浑浊.其余反应条件、部分反应物和生成物均已略去.试推断:
如图是初中化学中常见物质间的转化关系,其中甲、乙、丙为单质;A、B、C、D、E为同类化合物,且A与B的组成元素相同,D与E的组成元素也相同.已知C为红色固体、丙为黑色粉末,C和E在高温条件下可生成丙和D,D能使澄清的石灰水变浑浊.其余反应条件、部分反应物和生成物均已略去.试推断: