题目内容
10.在室温下,将53g质量分数为10%的碳酸钠溶液和3000g澄清石灰水充分混合,恰好完全反应,则这时所得NaOH溶液的质量是多少?(计算过程精确至0.1g)分析 碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠;由参加反应的碳酸钠溶液的质量、溶质的质量分数,根据反应的化学方程式进行分析解答即可.
解答 解:设生成碳酸钙沉淀质量为x
Ca(OH)2+Na2CO3═CaCO3↓+2NaOH
106 100
53g×10% x
则$\frac{106}{100}=\frac{53g×10%}{x}$,解得x=5g.
这时所得NaOH溶液的质量是53g+3000g-5g=3048g.
答:所得NaOH溶液的质量是3048g.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
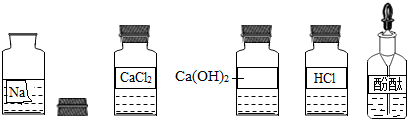
 2015年3月5目,国务院总理李克强在政府工作报告中指出:“努力建设生态文明的美好家园,推广新能源汽车…”
2015年3月5目,国务院总理李克强在政府工作报告中指出:“努力建设生态文明的美好家园,推广新能源汽车…”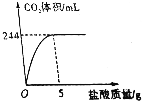 将20g稀盐酸加入到1.25g石灰石样品中反应,生成的CO2体积与加入盐酸质量的关系如图所示(已知本实验条件下CO2的密度为1.8g/L).
将20g稀盐酸加入到1.25g石灰石样品中反应,生成的CO2体积与加入盐酸质量的关系如图所示(已知本实验条件下CO2的密度为1.8g/L).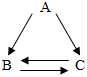 ABC代表单质或化合物,它们之间相互转换关系(如图所示);回答:
ABC代表单质或化合物,它们之间相互转换关系(如图所示);回答: