题目内容
19.有元素的化合价在化学反应前后发生了变化,则该反应为氧化还原反应.据此可判断下列化学反应属于氧化还原反应的是( )| A. | SO2+H2O═H2SO3 | B. | Na2CO3+2HCl═2NaCl+H2O+CO2↑ | ||
| C. | 2Al+3CuSO4═Al2(SO4)3+3Cu | D. | Fe2O3+3H2SO4=Fe2(SO4)3+3H2O |
分析 根据题意,有元素的化合价在化学反应前后发生了变化,则该反应为氧化还原反应,据此根据化合价的是否发生了变化判定哪些反应为氧化还原反应.
解答 解:A、SO2+H2O═H2SO3,反应前后各元素的化合价均不变,不属于氧化还原反应,故选项错误.
B、Na2CO3+2HCl═2NaCl+H2O+CO2↑,该反应是两种化合物相互交换成分生成两种新的化合物的反应,属于复分解反应,复分解反应的特征是反应前后元素的化合价不变,不属于氧化还原反应,故选项错误.
C、2Al+3CuSO4═Al2(SO4)3+3Cu,反应前后铝元素的化合价由0价变为+3价,铜元素的化合价由+2价变为0价,属于氧化还原反应,故选项正确.
D、Fe2O3+3H2SO4=Fe2(SO4)3+3H2O,该反应是两种化合物相互交换成分生成两种新的化合物的反应,属于复分解反应,复分解反应的特征是反应前后元素的化合价不变,不属于氧化还原反应,故选项错误.
故选:C.
点评 本题难度不大,考查同学们的新信息获取、处理能力,充分理解氧化还原反应的特征是正确解题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
19.下列实验操作正确的是( )
| A. |  闻气体气味 | B. |  点燃酒精灯 | C. |  滴加液体 | D. |  读取液体体积 |
14.小乐利用图甲所示装置测定空气中氧气的含量,其中燃烧匙内的白磷用电加热装置点燃,瓶内气压用气体压强传感器测定,其变化如图乙所示.则下列分析合理的是( )

| A. | t1时刻后的一段时间内瓶内气压显著增加,其原因是白磷燃烧产生大量白雾 | |
| B. | 从瓶内气压达到最高点直至t2时刻,瓶内温度始终保持不变 | |
| C. | 通过t2时刻瓶内的气压值,可以计算得出氧气约占空气体积的$\frac{1}{5}$ | |
| D. | t3时刻后的一段时间内瓶内气压又显著增加,其原因是气体的体积减小 |
4.下列实验操作图示正确的是( )
| A. |  熄灭酒精灯 | B. | 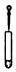 滴加液体 | C. | 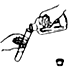 倾倒液体 | D. |  称量固体 |
8.下列物质中由离子构成的是( )
| A. | 氯化钠 | B. | 一氧化碳 | C. | 金刚石 | D. | 铜 |
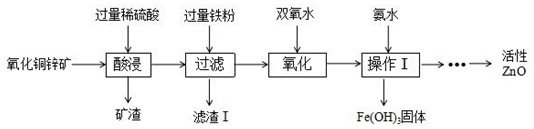
 如图为甲、乙、丙三种物质的溶解度曲线,回答下列问题:
如图为甲、乙、丙三种物质的溶解度曲线,回答下列问题: