题目内容
下表列出了KNO3在不同温度下的溶解度.
(1)由上表可推出KNO3溶解度曲线的变化规律是 .
(2)20℃时,把40g KNO3放入小烧杯,然后往烧杯中加入100g水并不断搅拌,则形成溶液的质量为 g;该溶液是 (填“饱和”或“不饱和”)溶液.
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
(2)20℃时,把40g KNO3放入小烧杯,然后往烧杯中加入100g水并不断搅拌,则形成溶液的质量为
考点:固体溶解度的影响因素
专题:溶液、浊液与溶解度
分析:(1)根据图表所给数据分析KNO3的溶解度随温度变化情况;
(2)根据20℃时KNO3的溶解度分析解答.
(2)根据20℃时KNO3的溶解度分析解答.
解答:解:(1)从图表可以看出,KNO3的溶解度随温度的升高而升高;
故答案为:KNO3溶解度随温度升高而增大(或“随温度降低而减少”).
(2)在20℃时,在100克水中最多能溶解31.6克的硝酸钾,所以形成溶液的质量是:100g+31.6g=131.6g.则所加的40g KNO3有一部分没有溶解,故该溶液是饱和溶液.
故答案是:131.6; 饱和
故答案为:KNO3溶解度随温度升高而增大(或“随温度降低而减少”).
(2)在20℃时,在100克水中最多能溶解31.6克的硝酸钾,所以形成溶液的质量是:100g+31.6g=131.6g.则所加的40g KNO3有一部分没有溶解,故该溶液是饱和溶液.
故答案是:131.6; 饱和
点评:固体物质的溶解度具备四要素:条件是温度一定;标准是100克溶剂;状态是饱和溶液;单位是克.

练习册系列答案
相关题目
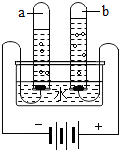 如图所示是电解水的实验装置图,请回答:
如图所示是电解水的实验装置图,请回答: 人类对原子结构的认识是逐渐深入的.如图是不同时期科学家提出的原子结构模型.
人类对原子结构的认识是逐渐深入的.如图是不同时期科学家提出的原子结构模型.
