题目内容
1.某小组为了验证Fe、Cu、Zn的金属活动性顺序,设计了如图1实验方案(该实验方案中所有金属均已打磨,且形状、大小以及稀硫酸的质量、浓度均相同):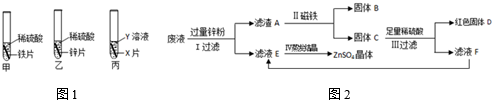
(1)小明同学设计的甲、乙实验可得出Zn的金属活动性比Fe强,依据的实验现象是铁表面产生气泡比锌表面产生气泡速率慢(填“快”或“慢”).
(2)甲、乙两个实验无法得出三种金属的活动性强弱,小聪同学补充设计了丙实验,他发现X片表面有红色固体析出,则丙实验中反应的化学方程式可以是Fe+CuSO4=FeSO4+Cu.
(3)小亮也设计了一套实验方案来证明Fe、Cu、Zn三种金属的活动性顺序,他选择的药品不可能是B(填序号).
A.Zn片 Cu片 FeSO4溶液
B.Cu片 FeSO4溶液 ZnSO4溶液
C.Fe片 Zn片 Cu片 H2SO4溶液
D.Fe片 ZnSO4溶液 CuSO4溶液
(4)实验完毕后,小李同学将含有CuSO4、ZnSO4、FeSO4、H2SO4等物质的废液倒在烧杯中,想回收工业重要原料硫酸锌和金属D.实验过程如图2:
①滤渣A中含有的金属有铁、铜、锌;
②步骤Ⅲ中发生的反应的化学方程式是Zn+CuSO4=ZnSO4+Cu,Zn+H2SO4=ZnSO4+H2↑;
③小李同学回收得到的金属D是铜.
分析 (1)根据金属越活泼,与酸反应越剧烈,生成气体速率越快进行分析;
(2)根据铁、锌和硫酸反应的现象可以验证两种金属的活动性顺序,只要再验证铁、铜的金属活动性顺序即可完成实验,所以X、Y可能分别是铁、铜盐,可以是铁、硫酸铜,铁和硫酸铜反应生成硫酸亚铁和铜进行分析;
(3)A、根据锌会与硫酸亚铁反应,铜不会与硫酸亚铁反应进行分析;
B、根据铜不会与硫酸亚铁、硫酸锌反应进行分析;
C、根据铁、锌与硫酸反应产生的气体速率不同,铜不会与硫酸反应进行分析;
D、根据铁会与硫酸铜反应,不会与硫酸锌反应进行分析;
(4)①根据过量的锌会与硫酸铜、硫酸亚铁稀硫酸反应,所以滤渣A中含有铁、铜、锌进行分析;
②根据过量的锌会与硫酸铜、硫酸亚铁稀硫酸反应,磁铁会吸引铁粉,所以固体C是锌,锌和硫酸反应会生成硫酸锌进行分析;
③根据铜不会与硫酸反应进行分析.
解答 解:
(1)金属越活泼,与酸反应越剧烈,生成气体速率越快,所以甲、乙实验得出Zn的金属活动性比Fe强,依据的实验现象是:依据的实验现象是铁表面产生气泡比锌表面产生气泡速率慢;
(2)铁、锌和硫酸反应的现象可以验证两种金属的活动性顺序,只要再验证铁、铜的金属活动性顺序即可完成实验,所以X、Y可能分别是铁、铜盐,可以是铁、硫酸铜,铁和硫酸铜反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO4=FeSO4+Cu;
(3)A、锌会与硫酸亚铁反应,铜不会与硫酸亚铁反应,故A正确;
B、铜不会与硫酸亚铁、硫酸锌反应,故B错误;
C、铁、锌与硫酸反应产生的气体速率不同,铜不会与硫酸反应,故C正确;
D、铁会与硫酸铜反应,不会与硫酸锌反应,故D正确;
故选:B;
(4)①过量的锌会与硫酸铜、硫酸亚铁、稀硫酸反应,所以滤渣A中含有铁、铜、锌;
②通过分析可知,过量的锌会与硫酸铜、硫酸亚铁稀硫酸反应,磁铁会吸引铁粉,所以固体C是锌,锌和硫酸反应会生成硫酸锌和氢气,化学方程式为:Zn+CuSO4=ZnSO4+Cu,Zn+H2SO4=ZnSO4+H2↑;
③通过分析可知,铁被磁铁吸引,锌和稀硫酸反应,铜不会与硫酸反应,所以回收得到的金属D是铜.
故答案为:
(1)慢;
(3)Fe+CuSO4=FeSO4+Cu;
(4)Cu、Fe、Zn;
(5)B;
(4)①铁、铜、锌;
②Zn+CuSO4=ZnSO4+Cu,Zn+H2SO4=ZnSO4+H2↑;
③铜.
点评 金属活动性顺序的应用主要表现在两个方面:一是只有排在氢前面的金属才能与酸反应,生成氢气和盐(位置越靠前,反应越剧烈),二是金属与盐溶液的反应时,只有排在前面的金属才能将排在它后面的金属从它的盐溶液中置换出来.

| A. | 用小苏打碳酸钠治疗胃酸过多症 | |
| B. | 人体的头发主要成分是蛋白质,容易受酸性溶液侵蚀 | |
| C. | 用碳酸钙作牙膏的摩擦剂 | |
| D. | 用pH试纸测定某地雨水的pH为0,此雨水为酸雨 |
 实验室中有一瓶标签受损的无色液体,如图所示.这瓶无色液体是什么呢?实验员老师告诉大家,该液体只能是过氧化氢溶液、稀硫酸.
实验室中有一瓶标签受损的无色液体,如图所示.这瓶无色液体是什么呢?实验员老师告诉大家,该液体只能是过氧化氢溶液、稀硫酸.为确定该液体成分,同学们继续进行了如下实验探究:
| 实验操作 | 实验现象 | 实验结论 |
| 步骤一:取该液体适量于试管中,向其中加入少 量二氧化锰粉末. | 没有气泡产生. | 该液体不是过氧化氢溶液. |
| 步骤二:取该液体适量于试管中,向其中滴加少量硝酸钡溶液. | 有白色沉淀生成 | 该液体是稀硫酸. |
| A. | 滤纸上有Ag、Cu,滤液中有Zn(NO3)2、Mg(NO3)2 | |
| B. | 滤纸上有Ag、Cu、Zn,滤液中有Zn(NO3)2、Mg(NO3)2 | |
| C. | 滤纸上有Ag、Cu,滤液中有AgNO3、Zn(NO3)2、Mg(NO3)2 | |
| D. | 滤纸上有Ag,滤液中有AgNO3、Cu(NO3)2、Zn(NO3)2、Mg(NO3)2 |

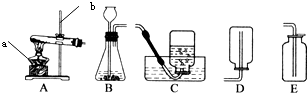 实验室常用如图所示装置来制取氧气:
实验室常用如图所示装置来制取氧气:
 小科以化合价为纵坐标、以物质类别为横坐标绘制了如图,每种物质中都有一种元素的化合价与纵坐标的数值对应,图中字母均表示初中科学中的常见物质,其中“→”表示物质间的转化关系.已知A为硫的氧化物且氧元素的质量分数为60%,C、D、E、F均含有铜元素.请回答:
小科以化合价为纵坐标、以物质类别为横坐标绘制了如图,每种物质中都有一种元素的化合价与纵坐标的数值对应,图中字母均表示初中科学中的常见物质,其中“→”表示物质间的转化关系.已知A为硫的氧化物且氧元素的质量分数为60%,C、D、E、F均含有铜元素.请回答: